
| A. | 滴水成冰 | B. | 死灰复燃 | C. | 积土成堆 | D. | 立竿见影 |
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
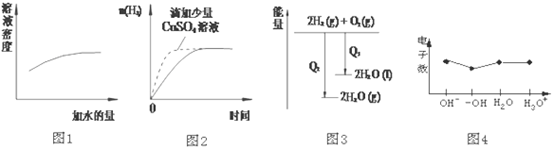
| A. | 图1表示浓硫酸的稀释 | |
| B. | 图2表示过量的盐酸与等量的锌粉反应 | |
| C. | 图3表示氢气与氧气反应中的能量变化 | |
| D. | 图4表示微粒电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
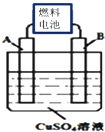 短周期主族元素A,B,C,D,E,F的原子序数依次增大,它们的原子核外电子层数之和为13.B的化合物种类繁多,数目庞大;C,D是空气中含量最多的两种元素,D,E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素.试回答以下问题:
短周期主族元素A,B,C,D,E,F的原子序数依次增大,它们的原子核外电子层数之和为13.B的化合物种类繁多,数目庞大;C,D是空气中含量最多的两种元素,D,E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素.试回答以下问题: ,A、C、F三种元素形成的化合物CA4F为离子化合物(填“离子”或“共价”).
,A、C、F三种元素形成的化合物CA4F为离子化合物(填“离子”或“共价”).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 刚玉--SiO2 | B. | 明矾--Al2(SO4)3•12H2O | ||
| C. | 小苏打--Na2CO3 | D. | 漂白粉--Ca(ClO)2、CaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用丁达尔效应区分淀粉溶液和食盐水 | |
| B. | 用品红溶液区分SO2与CO2气体 | |
| C. | 用石蕊试液区分KOH溶液与NaOH溶液 | |
| D. | 用碘水区分淀粉溶液与蛋白质溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 结论 |
| 在一杯浑浊的水中加 少量Al2(SO4)3静置 | 烧杯中的水变澄清 | Al2(SO4)3可 以净水 |
| 在一杯浑浊的水中加 少量KCl,静置 | 烧杯中的水 仍然浑浊 | K+不能起净水作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
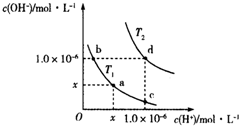
| A. | T2>25℃ | B. | x=1.0×10-7 | ||
| C. | KW(a)=KW(d) | D. | b点溶液呈碱性,c点溶液呈酸性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com