
����Ŀ���ȱ���Ⱦ�ϡ�ҽҩ���л��ϳɵ��м��壬����Ҫ���л�������Ʒ����ϳɷ�Ӧԭ���ǣ�C6H6+Cl2![]() C6H5Cl+HCl
C6H5Cl+HCl
ijʵ������ȡ�ȱ���װ����ͼ��ʾ�����Ⱥͼг�װ������ȥ����
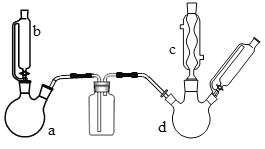
��ش��������⣺
(1)����a��b��ϳ���ȡ������װ�ã���Ӧ����Ҫ���ȣ�������a�еĹ��巴Ӧ����__���ѧʽ����
(2)�����������ͨ��װ��40mL�����ܶ�0.88g/mL���ķ�Ӧ��d�У�������м����������ά�ַ�Ӧ�¶���50��60�棬����40���ӡ�������d���ȵķ�����__��
(3)����c��������___������c���ڵ�����ɷ���HCl��Cl2��__��
(4)��d�е�Һ�嵹���Һ©���У��ֱ�������ˮ��NaOH��Һϴ�ӣ�������IJ����������������õ�24g�������ȱ���
�ټ�ϴ֮ǰҪ����ˮϴ����Ŀ����__��
����10%NaOH��Һ��ϴʱ����������ԭ��Ӧ�Ļ�ѧ����ʽΪ__��
�۸�ʵ�������ȱ��IJ���Ϊ__������С�����һλ�����ò��ʵ������۲��ʵ�ԭ��___����д��������
���𰸡�KMnO4 ˮԡ���� ���������� ������ ϴȥ��Ʒ�е�FeCl3��HCl����ʡ������������ͳɱ� Cl2��2NaOH=NaCl��NaClO��H2O 47.2%����47.3%�� �ȱ�����ȡ����������ʧ���и���Ӧ����
��������
����a��b��ϳ���ȡ������װ�ã���Ӧ����Ҫ���ȣ���ӦΪKMnO4��Ũ���ᷴӦ��Cl2��������Ӧ�Ļ�ѧ����ʽΪ2KMnO4+16HCl(Ũ)=2KCl+2MnCl2+5Cl2��+8H2O��a��d���ϴ��ƿ��Ӧװ��Ũ���ᣬ���ڳ�ȥCl2�л��е�ˮ��������d�У�����������ͨ��װ��40mL�����ܶ�0.88g/mL���ķ�Ӧ��d�У�������м��������������Ҫά�ַ�Ӧ�¶���50��60���������������ˮԡ���ȡ����ɵ��ȱ��л��б���Cl2��HCl��FeCl3�ȣ���ˮϴȥ��HCl��FeCl3�ȣ�����NaOHϴ�ӣ�ȥ��Cl2��Ȼ���Һ���ٽ��������Ա��ô������ȱ���
(1)����a��b��ϳ���ȡ������װ�ã���Ӧ����Ҫ���ȣ���ӦΪ����KMnO4��Ũ���ᷴӦ��ȡ������������a�еĹ��巴Ӧ����KMnO4����Ϊ��KMnO4��
(2)����ά�ַ�Ӧ�¶���50��60�������Կ�������ˮԡ���ȣ�������d���ȵķ�����ˮԡ���ȡ���Ϊ��ˮԡ���ȣ�
(3)����c�����������������ܣ����ӷ�����������c���ڵ�����ɷ���HCl��Cl2�ͱ���������Ϊ�����������ܣ���������
(4)����HCl��FeCl3������ˮ��Ϊ��ʡ��Һ���ڼ�ϴ֮ǰҪ����ˮϴ����Ŀ����ϴȥ��Ʒ�е�FeCl3��HCl����ʡ������������ͳɱ�����Ϊϴȥ��Ʒ�е�FeCl3��HCl����ʡ������������ͳɱ�
����10%NaOH��Һ��ϴʱ����ҪϴȥCl2��Cl2��NaOH��Һ��Ӧ������NaCl��NaClO�ȣ�����������ԭ��Ӧ�Ļ�ѧ����ʽΪCl2��2NaOH=NaCl��NaClO��H2O����Ϊ��Cl2��2NaOH=NaCl��NaClO��H2O��
�۱���������Ӧ���ȱ���ѧ����ʽΪ![]() +Cl2
+Cl2![]()
![]() +HCl�����������Ƶ��ȱ�������Ϊ
+HCl�����������Ƶ��ȱ�������Ϊ![]() =50.77g����ʵ�������ȱ��IJ���Ϊ
=50.77g����ʵ�������ȱ��IJ���Ϊ![]() =47.2%����47.3%�����ò��ʵ������۲��ʵ�ԭ���ȱ�����ȡ����������ʧ���и���Ӧ��������Ϊ��47.2%����47.3%�����ȱ�����ȡ����������ʧ���и���Ӧ������
=47.2%����47.3%�����ò��ʵ������۲��ʵ�ԭ���ȱ�����ȡ����������ʧ���и���Ӧ��������Ϊ��47.2%����47.3%�����ȱ�����ȡ����������ʧ���и���Ӧ������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�ڻ�ѧʵ�����ж�����;��

(1)���ô�װ���ռ������������_____��ͨ�룬���ô�װ���ռ������������____��ͨ�롣
(2)����λͬѧ������ˮ���ռ���������װ����ͼ��

�����_______��ͨ�룬�ϲ�Һ��Ӧѡ��_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʿռ�վ����CO2��һ����Ҫ�����ǽ�CO2��ԭ�����漰�ķ�Ӧ����ʽΪ��CO2(g) + 4H2(g)![]() CH4(g) + 2H2O(g)�����¶ȴ�300������400������Ӧ���´ﵽƽ��ʱ��H2������������������й��ڸù��̵��ж���ȷ����
CH4(g) + 2H2O(g)�����¶ȴ�300������400������Ӧ���´ﵽƽ��ʱ��H2������������������й��ڸù��̵��ж���ȷ����
A. �÷�Ӧ����H < 0 B. ��ѧƽ�ⳣ��K����
C. CO2��ת�������� D. ����Ӧ���������淴Ӧ���ʼ�С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦN2O4��g��![]() 2NO2��g����H=+57kJmol��1�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�ı仯������ͼ��ʾ������˵����ȷ����
2NO2��g����H=+57kJmol��1�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�ı仯������ͼ��ʾ������˵����ȷ����

A.a��c���������ƽ����Է���������a��c
B.a��c�����������ɫ��a�cdz
C.��״̬b��״̬a�������ü��ȵķ���
D.a��c����ķ�Ӧ���ʣ�a��c
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼��Ԫ�صĵ��ʼ��仯��������������������һ����Ҫ���ʡ���ش���������
(1)̼ԭ�Ӻ�����__�ֲ�ͬ�˶�״̬�ĵ��ӣ���һ�����ܽ������̼֮���Ԫ�ص�����Ϊ__��̼��Ԫ����Χ�����Ų���ͨʽΪ__��
(2)�����أ�C15H22O5���Ľṹ��ͼ��ʾ��ͼ�����ֱ�ʶ�����̼ԭ�ӵ��ӻ��������Ϊ__����������ص�����Ԫ�ص縺���ɴ�С������__��

(3)�����ط����У���Ԫ�صijɼ���ʽ��___������������ȡ�����ص�����ܼ���___��
a���Ҵ� b������ c��ˮ
(4)SnO2��һ����Ҫ�İ뵼�崫�������ϣ������Ʊ������ȸߵ�������������SnO2������NaOH��Ӧ����Na2SnO3��Na2SnO3�������ӿռ乹��Ϊ__��
(5)������̫���ܵ�������л�����±����⻯Ǧ�װ�(CH3NH3PbI3����Է�������ΪMr)�뵼����Ϊ������ϣ�CH3NH3PbI3���и��ѿ�(AMX3)�������ṹ���侧����ͼ��ʾ��AMX3�����������������(M)���������±��������(X)�γ���������ṹ����X����__λ�á�CH3NH3PbI3����ľ�������Ϊanm���侧���ܶ�Ϊdg��cm-3�����ӵ�������ֵNA�ļ������ʽΪ__��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1molH2(g)��1molI2(g)��Ӧ����HI(g)�ͷų�8.7kJ�������й�������ͼ��ʾ��
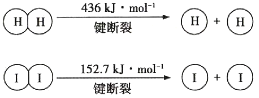
����˵������ȷ���ǣ� ��
A.H2��I2������������HI������
B.�ƻ�1molH��I����Ҫ��������298.7kJ
C.1molHI(g)��ȫ�ֽ�����H2(g)��I2(g)ʱ����4.35kJ����
D.H2(g)�е�H��H����HI(g)�е�H��I���ι�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������̼������ʱ�У�Ҳ�ǻ���Ҫ������̼���ڹ�ҵ�����������ش������ԭ���ϣ����ŷŻ�����ŷ�������������ͬ����������������ȶ��Ǻܺõ�����̼��������ʽ�������Ǽ����������÷�����������Һ������������������淋Ĺ��գ�

��ش��������⣺
��1�����ղ����������ֱ�Ϊ____________��____________��
��2����ҵ�ϳɰ��Ļ�ѧ����ʽΪ��__________��
��3��д����������Ʒ�������ӷ���ʽ��________��
��4����ʵ�����м���ϳɰ����ų��ķ������Ƿ��а����ķ�����______________��
��5������Ʒ�Ļ�ѧʽΪ________________�����������������п���ѭ��ʹ�õ�������__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������õ���Դ���ޣ���˵�Ĺ�ҵ��������Ҫ���塣��ͼ��ij�о�С����ƵĴ�ʵ���Һ����Һ(��Ҫ����![]() ��
��![]() �͵��۵�)�л��ջ�øߴ��⾧������̡�
�͵��۵�)�л��ջ�øߴ��⾧������̡�
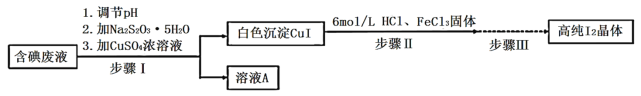
��֪��![]() ��
��![]() ��ʵ��������
��ʵ��������![]() ����
����![]() ����������ԭ��Ӧ���ش��������⣺
����������ԭ��Ӧ���ش��������⣺
(1)����I�У���װ�к����Һ���ձ��У��ȼ���![]() ���壬�ڽ������ܽ����������������ͭ��Һ������ͭ��������________��
���壬�ڽ������ܽ����������������ͭ��Һ������ͭ��������________��
(2)�����йز���I��˵����ȷ����_________________��
A.ʵ����Ӧ����![]() Ϊǿ���Ի���
Ϊǿ���Ի���
B.![]() ��Һ��������
��Һ��������![]() ������룬��Ϊ�˷�ֹ���ɵĵ�ӷ�����ʧ
������룬��Ϊ�˷�ֹ���ɵĵ�ӷ�����ʧ
C.������������Ƶ���Ӧ�����������Һ����ɫ�պ���ȥ
D.��Һ![]() �к���Ԫ�ص����ӿ�����
�к���Ԫ�ص����ӿ�����![]() ��
��![]() ��
��![]() ��
��
(3)�����Ϊ��Ӧ���ɵⲢ�������Ĺ��̣�ʾ��ͼ��ͼ��ʾ��
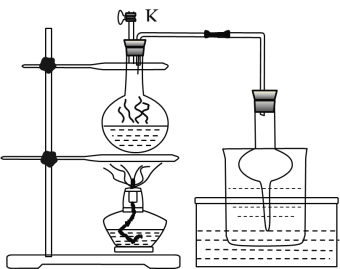
��д�����������ӷ���ʽ________��
�ڲ�����װ��������(��ʱ![]() �ر�)����Բ����ƿ�м���
�ر�)����Բ����ƿ�м���![]() ��
��![]() ���弰����
���弰����![]() ��������IJ���˳����________��(ѡ�����������������)
��������IJ���˳����________��(ѡ�����������������)
a.��![]() b.�ر�
b.�ر�![]() c. �þƾ��Ƽ��� d. ֹͣ���� e. �۲쵽Բ����ƿ����Һ��ɫ��ʧ
c. �þƾ��Ƽ��� d. ֹͣ���� e. �۲쵽Բ����ƿ����Һ��ɫ��ʧ
��ʵ����ڣ����ֲ������������⾧�����ᣬ�䴦���ļ��ײ�������________��
(4)������У���Ҫ�漰�IJ��������dz��ˡ�ϴ�ӡ������________�����У����ˡ�ϴ�ӳ��������ֽ���ܶ�����Ӧ���������������У���ԭ����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ��Ϊ�Ƚ�þ�����Ľ�����ǿ�������������ʵ�飺
��1������֧�Թ��зֱ����3 mLͬŨ�ȵ�ϡ���ᣬ�ٽ������С��ͬ�Ҵ�����þƬ����Ƭ�ֱ�����Թ��У���Ӧ��ʼʱ�۲쵽��ͼ��ʾ���������Թ�b�ڼ���Ľ���Ϊ____________��д��ѧʽ����

��2���������������������ʵ�����ȣ����Թ���ϡ������������ַ�Ӧ������״̬Ҳ����ͼ��ʾ�����Թ�b�з�Ӧ�����ӷ���ʽΪ___________��
��3�������жϣ�ʵ��________[������1����������2����]��֤��þ�Ľ�����ǿ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com