
【题目】某金属与稀硝酸反应生成一种硝酸盐,该硝酸盐受热分解生成NO2、O2和一种固体,该固体中金属元素的化合价比原硝酸盐中该金属的化合价高,则该硝酸盐分解后生成的NO2和O2的物质的量之比为 ( )
A. 8∶1 B. 4∶1 C. 2∶1 D. 1∶1
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某有机物分子式为C4H8,据此推测其结构和性质不可能的是 ( )
A.它与乙烯可能是同系物
B.一氯代物可能只有一种
C.分子结构中甲基的数目可能是0、1、2
D.等质量CH4和C4H8分别在氧气中完全燃烧,CH4的耗氧量小于C4H8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】油脂不仅是营养物质和主要食物,也是一种重要的上业原料。下面是以油脂为主要原料获得部分产品的合成路线:
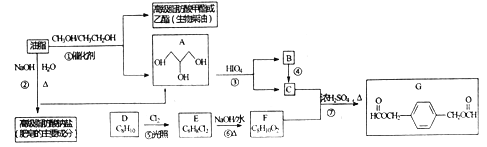
已知:
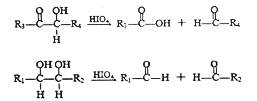
(R1、R2、R3与R4可能是氢、烃基或其他基团)
回答下列问题:
(1)下列关于油脂的说法正确的是____________. (填标号)
a.油脂包括植物油和脂肪,属于酯类
b.天然油脂是混合物,无固定的熔点和沸点
c.油脂属天然高分子化合物
d.硬化油又叫人造脂肪,便于储存和运输,但容易被空气氧化变质
(2)G中官能团的名称为________,反应①的反应类型为__________
(3)用系统命名法写出A的名称__________, C与F反应生成G的化学方程式为_____。
(4)二元取代芳香化合物H是G的同分异构体,H满足下列条件:
① 能发生银镜反应,② 酸性条件下水解产物物质的最之比为2: 1,③ 不与NaHCO3溶液反应。
则符合上述条件的H共有_____种(不考虑立体结构,不包含G本身),其中核磁共振氢谱为五组峰的结构简式为_________________(写出一种即可)。
(5)写出从HOCH2CH2OH![]() HCOOCH2CH2OOCH 的合成路线(无机试剂任选,合成路线参照题中的书写形式)________________。
HCOOCH2CH2OOCH 的合成路线(无机试剂任选,合成路线参照题中的书写形式)________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,集气瓶内充满某混合气体,将集气瓶置于光亮处,然后挤压胶头滴管使胶头滴管内的水进入集气瓶,发现烧杯中的水会倒吸进入集气瓶,则集气瓶内的混合气体可能是

①CO、O2 ②NO、O2 ③NO2、O2④N2、H2 ( )
A. ①② B. ②④
C. ③④ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在饱和氯水中存在平衡:Cl2+H2O![]() H++Cl-+HClO,下列叙述中正确的是( )
H++Cl-+HClO,下列叙述中正确的是( )
A.用pH试纸测得溶液pH<7
B.向其中加入AgNO3溶液,平衡向右移,溶液的pH变小
C.向其中加入NaOH使pH=7,所得溶液中微粒浓度的关系如下:c(Na+)>c(Cl-)>c(ClO-)=c(HClO)
D.若氯水久置pH会逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食醋的总酸量即一定体积的食醋原液所含醋酸的质量,单位是g· L-1或个g/100mL。国家标准规定酿造食醋总酸含量不得低于3.5g/100mL。
(1)用酸碱滴定法测定某食醋样品中的总酸量时,下列说法中正确的是 。
A.用NaOH溶液滴定时反应的离子方程式为H++OH-=H2O
B.食醋样品不需要预先稀释一定倍数后可以直接进行滴定
C.用NaOH溶液滴定时,可使用酚酞或甲基橙作指示剂
D.若测得样品的物质的量浓度为0.75mol·L-1,则其总酸量为45g·L-1
(2)某同学仔细观察该食醋样品的标签,发现其中还含有作为食品添加剂的苯甲酸钠(C6H5COONa),他想用理论验证醋酸与苯甲酸钠不会发生离子互换反应,需查找在一定温度下醋酸与苯甲酸的 。
A.pH B.电离度 C.电离常数 D.溶解度
(3)常温下,用0.1000mol· L-1 NaOH溶液分别滴定20.00mL 0.1000mol· L-1 HCl溶液和20.00mL 0.1000mol· L-1 CH3COOH溶液,得到两条滴定曲线,如图所示。
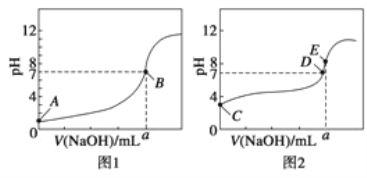
①滴定醋酸溶液的曲线是 (填“图1”或“图2”);滴定曲线中a= mL;
②E点pH>8的原因是(用离子方程式表示): 。
(4)测定食醋的总酸量实验中,配制NaOH溶液和稀释食醋所用的蒸馏水必须煮沸,目的是 。
(5)实验时,吸取食醋样品10mL于100mL容量瓶中定容。移取定容后的溶液20mL于锥形瓶中,加入1~2滴指示剂,用浓度为c mol·L-1的NaOH标准溶液滴定,平行测定三次,消耗NaOH溶液的平均体积为V mL。则原食醋样品的总酸量=____________g/100mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学研究性学习小组查阅资料了解到以下内容:
乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸,其熔点为101.5℃,在157℃升华。为探究草酸的部分化学性质,进行了如下实验:
(1)向盛有1 mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生。该反应的离子方程式为___________________________。
(2)向盛有乙二酸饱和溶液的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去,说明乙二酸具有________(填“氧化性”、“还原性”或“酸性”),请配平该反应的离子方程式:
_____MnO4-+_____H2C2O4+____H+ = ____Mn2++_____CO2+____H2O
(3)将一定量的乙二酸放于试管中,按下图所示装置进行实验(夹持装置未标出):
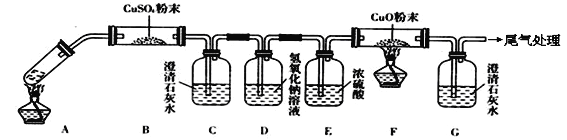
实验发现:装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末变红。据此回答:
上述装置中,D的作用是______。乙二酸分解的化学方程式为__________。
(4)该小组同学将2.52g草酸晶体(H2C2O4·2 H2O)加入到100mL0.2mol·L-1的NaOH溶液中充分反应,测得反应后溶液呈酸性,其原因是_______(用文字简单描述)。
(5)以上溶液中各离子的浓度由大到小的顺序为:_________(用离子符号表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com