
【题目】(1)人的纯净胃液是一种无色而呈酸性的液体,pH在0.9~1.5之间,胃液中含有大量盐酸,其中的H+浓度比血液高几百万倍,试回答下列问题:
①若胃液酸度增高就患胃酸过多症,下列物质不宜用作治疗胃酸过多症药物的主要成分的是(____)
A.小苏打粉 B.氢氧化铝粉 C.氧化钙粉 D.纯碳酸钙粉
②胃溃疡患者胃酸过多可考虑选用①中的 ________________。(填字母编号)写出反应的化学方程式______________________________ 。
(2)现有下列四种物质:A.食盐B.食醋 C.苹果汁 D.葡萄糖,请按下列要求填空(填序号)。
富含维生素C的是_________;可直接进入血液补充能量的是_________;即可作为调味剂,又可预防感冒的是_________;食用过多会引起血压升高、肾脏受损的________。
(3)保护环境、呵护地球已成为为类共同的呼声。
①水是一种宝贵的资源,保护水资源就是保护我们的生命。下列做法不利于水资源保护的是__________(填字母编号);
A.科学合理使用农药 B.任意排放化工厂废水 C.处理生活污水,达标排放
②矿泉水瓶不能随意丢弃。根据垃圾分类方法,矿泉水瓶属于__________(填“可回收物”或“可堆肥垃圾”);
【答案】 C B ![]() C D B A B 可回收物
C D B A B 可回收物
【解析】(1)选择治疗人体疾病的药物,既要考虑药物的效果,又要考虑药物对人体的副作用的大小;根据质量守恒定律可以书写化学方程式;
(2)根据物质含有的主要成分、性能和用途结合问题解答;
(3)根据能引起水体污染的来源分析;根据矿泉水瓶的主要成分判断。
(1)①氧化钙虽然能和盐酸反应,但是氧化钙溶于水时放出大量的热,对人体副作用很大,因此不宜用作治疗胃酸过多症药物,答案选C。
②碳酸盐能与盐酸反应产生二氧化碳气体,因此不宜用作治疗胃溃疡患者胃酸过多,应该用氢氧化铝,答案选B。反应的化学方程式为Al(OH)3+3HCl=AlCl3+3H2O。
(2)富含维生素C的是苹果汁;可直接进入血液补充能量的是葡萄糖;食醋中含有醋酸,即可作为调味剂,又可预防感冒;食用过多会引起血压升高、肾脏受损的是氯化钠。
(3)①生活用水、工业废水、农药和化肥的不合理使用都能造成地下水的污染,因此科学合理使用农药、处理生活污水,达标排放是保护水资源的有效措施,答案为B;
②矿泉水瓶的主要成分是聚对苯二甲酸乙二醇酯,是食品用塑料瓶,属于可回收物。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值。下列叙述正确的是
A. 1molAlCl3在熔融状态时含有的离子总数为0.4NNA
B. 1molOH-与17gNH3所含的电子数分别为9NA和10NA
C. 常温常压下,0.1molNH3与0.1molHCl充分反应后所得的产物中含有的分子数为0.1NA
D. 13.8gNO2与足量水反应,转移的电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含Na2SO4、NaCl、MgCl2的1L混合溶液c (Na+) = 0.5 mol/L,c(Cl-)=0.4 mol/L,c(Mg2+)= 0.15 mol/L则此溶液中c (SO42-)为
A.0.15 mol/LB.0.2 mol/L
C.0.3 mol/LD.0.4 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小明同学想通过比较两种最高价氧化物水化物的酸性强弱来验证S与C的非金属性的强弱,他查阅了资料:可以利用强酸制备弱酸的原理来判断酸性强弱。于是小明采用了下图所示的装置进行实验。请回答:

(1)仪器A的名称是________,应盛放下列药品中的__________。
a.稀硫酸 b.亚硫酸 c.氢硫酸 d.盐酸
(2)仪器B的名称是________,应盛放下列药品中的__________。
a.碳酸钙 b.硫酸钠 c.氯化钠 d.碳酸钠
(3)仪器C中盛放的药品是澄清石灰水,如果看到的现象是澄清石灰水变浑浊,证明B中发生反应生成了_____________,即可说明___________比________酸性强,非金属性________比______强,B中发生反应的离子方程式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.10mol/L的盐酸分别滴定体积相同且浓度均为0.10mol/L的三种一元碱XOH、YOH及ZOH,滴定曲线如图所示。

下列说法正确的是
A. 滴定XOH时可用酚酞作指示剂
B. YOH是强碱
C. X++H2O![]() XOH+H+的平衡常数K=10-4
XOH+H+的平衡常数K=10-4
D. [V(盐酸)/V(碱)]=0.5时,c(Z+)>c(Y+)>c(X+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸铜易溶于水,在130℃时会发生分解反应,是一种燃烧催化剂。以食盐等为原料制备高氯酸铜[Cu(ClO4)2·6H2O]的一种工艺流程如下:
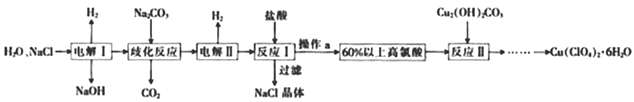
(1)发生“电解I”时,所用的交换膜是_______________(填“阳离子交换膜”或“阴离子交换膜”)。
(2)歧化反应是同一种物质中同种元素自身的氧化还原反应,已知上述工艺流程中“歧化反应”的产物之一为NaClO3。
①“歧化反应”的化学方程式为____________________________。
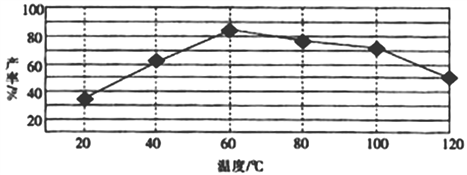
②“歧化反应”阶段所采用的不同温度对产率影响的结果如图所示。则该反应最适宜的温度是___。
(3)“电解II”的阳极产物为______________(填离子符号)。
(4)操作a的操作名称是_______,该流程中可循环利用的物质是_____________(填化学式)。
(5)用该工艺流程制备高氯酸铜时,若起始时NaCl的质量为at,最终制得的Cu(ClO4)2·6H2O为bt,则产率为__________(用含a、b的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 25℃,1L pH=13的NaOH溶液中含有OH-的数目为0.1NA
B. 常温常压下,17g甲基(—14CH3)所含的中子数9NA
C. 标准状况下,1L己烷充分燃烧后生成的气态产物的分子数为![]() NA
NA
D. 1mol乙酸(忽略挥发损失)与足量的C2H518OH在浓硫酸作用下加热,充分反应可生成NA个CH3CO18OC2H5分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com