
【题目】氮及其化合物广泛存在于自然界中,回答下列问题:
(1)基态氮原子核外有________种不同运动状态的电子,其价层电子排布图为_______________
(2)NH4NO3中元素的第一电离能大小关系:N_______ O,NO3-的空间构型为___________,NH4+中氮原子的杂化类型为_________
(3)HCN分子中含______个σ和________个π键。与CN-互为等电子体的分子和离子分别为______和______(各举一例,填化学式)
(4)NH3极易溶于水,其主要原因是__________________________________________________________________
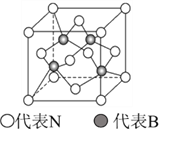
(5)立方氮化硼的结构与金刚石相似,其晶胞如图所示,B原子周围最近的N原子所构成的立体图形为_________,一个晶胞中N原子数目为__________
【答案】 7 ![]() > 平面三角形 sp3 2 2 CO或N2 C22-或O22+或NO+ NH3与H2O均为极性分子,且相互间能形成氢键,因此NH3极易溶于水 正四面体 4
> 平面三角形 sp3 2 2 CO或N2 C22-或O22+或NO+ NH3与H2O均为极性分子,且相互间能形成氢键,因此NH3极易溶于水 正四面体 4
【解析】(1)氮是7号元素,基态氮原子核外有7种不同运动状态的电子,其价层电子排布图为![]() ,故答案为:7;
,故答案为:7;![]() ;
;
(2)N的2p为半充满结构,第一电离能较大,第一电离能:N>O,NO3-中N的价层电子对数=3+![]() (5+1-3×2)=3,采用sp2杂化,空间构型为平面三角形,NH4+中氮原子的价层电子对数=3+
(5+1-3×2)=3,采用sp2杂化,空间构型为平面三角形,NH4+中氮原子的价层电子对数=3+![]() (5-1-4×1)=4,采用sp3杂化,故答案为:>;平面三角形;sp3;
(5-1-4×1)=4,采用sp3杂化,故答案为:>;平面三角形;sp3;
(3)HCN分子的结构式为H-C≡N,其中含2个σ和2个π键。与CN-互为等电子体的分子和离子分别为CO或N2、C22-,故答案为:2;2;CO或N2;C22-;
(4)NH3与H2O均为极性分子,且相互间能形成氢键,因此NH3极易溶于水,故答案为:NH3与H2O均为极性分子,且相互间能形成氢键,因此NH3极易溶于水;
(5)根据晶胞结构图,B原子周围最近的4个N原子构成正四面体结构,一个晶胞中N原子数目=8×![]() +6×
+6×![]() =4,故答案为:正四面体;4。
=4,故答案为:正四面体;4。


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】黄铜灰渣(含有Cu、Zn、CuO、ZnO 及少量的FeO、Fe2O3) 生产氯化铜晶体的流程如下:
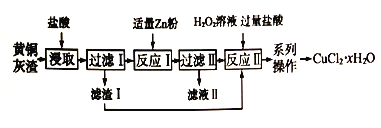
(1)反应I中所加Zn 粉不能过量的原因是_____________。
(2)滤液I中含有的主要金属阳离子是_____________。
(3) 写出反应II 的化学方程式_____________。
(4)“系列操作”包括蒸发浓缩、冷却结晶、过滤、______、_____。
(5) 在空气中直接加热CuCl2·xH2O晶体得不到纯的无水CuCl2,原因是_____________。
(6) 298K 时,向c (Cu2+) =0.02mol/L的溶液中加入氢氧化钠来调节溶液的pH,若反应后溶液pH=10,此时Cu2+是否沉淀完全? _____{列式计算,己知:Ksp[Cu(OH)2] =2.2×10-20,c(Cu2+)<1×10-5mol/L 视为沉淀完全}_____。
(7) CuCl2·xH2O晶体中x值的测定:称取3.420 g 产品溶解于适量水中,向其中加入含AgNO34.400×10-2mol 的AgNO3溶液(溶液中除Cl- 外,不含其他与Ag+反应的离子),待C1-完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol/L 的KSCN 标准溶液滴定剩余的AgNO3。使剩余的Ag+以AgSCN 白色沉淀的形式析出。
①滴定终点的现象是__________。
②若滴定过程用去上述浓度的KSCN 标准溶液20.00mL,则CuCl2·xH2O中x值为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如下图所示。下列说法正确的是( )
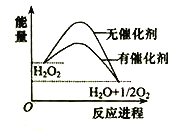
A. 加入催化剂,减小了反应的热效应
B. 加入催化剂,可提高H2O2的平衡转化率
C. H2O2分解的热化学方程式:H2O2 → H2O + O2 + Q
D. 反应物的总能量高于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)1mol H2SO4中含___________ 个硫原子,___________mol氧原子。
(2)标准状况下,①1.7g氨气、②3.36 L甲烷、③6.02×1022个二氧化碳分子,含原子数最多的是(填序号,下同)________,质量最大的是_________。
(3)9g某二价金属的氯化物ACl2中含有0.2mol Cl-离子,则ACl2的摩尔质量___________;
(4)某双原子分子构成的气体,其摩尔质量为M g/mol,该气体质量为m g,阿伏加德罗常数为NA,则:
①该气体在标准状况下的体积为__________L;
②该气体的一个分子的质量为__________ g;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在3个体积均为1.0 L的恒容密闭容器中反应2H2(g)+CO(g)![]() CH3OH(g) 达到平衡。下列说法正确的是
CH3OH(g) 达到平衡。下列说法正确的是
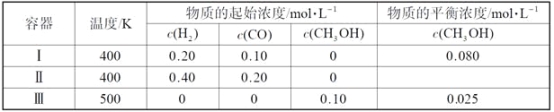
A. 该反应的正反应放热
B. 达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大
C. 达到平衡时,容器Ⅱ中c(H2)大于容器Ⅲ中c(H2)的两倍
D. 达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化反应与还原反应在同一元素中进行的是( )
A. Cl2+2NaOH=NaCl+NaClO+H2O
B. Fe+CuSO4=FeSO4+Cu
C. 2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
D. 2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】席夫碱类化合物G有机合成、药物、新材料等方面有广泛应用。合成G的一种路线如下:
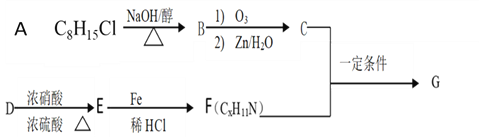
①![]()
②1molB经上述反应可生成2molC,且C不能发生银镜反应
③D属于单取代芳烃,其相对分子质量为106
④核磁共振氢谱显示F苯环上有两种化学环境的氢
⑤![]()
回答下列问题:
(1)B的化学名称_________________,A生成B的化学方程式___________________________________
(2)A 生成B , E 生成F的反应类型分别是__________,___________
C+F 生成G的化学方程式________________________________________________________________
(3)E的同分异构体中,含有苯环和氨基且能与碳酸氢钠反应生成CO2的共有_______种,其中核磁共振氢谱有五组峰,峰面积之比为1:2:2:2:2的结构简式为________________________(任意写一种)
(4)已知![]() 请以乙烯为原料,其他试剂任选,写出合成吸水材料聚丙烯酸钠的合成路线___________________________________________________________________________
请以乙烯为原料,其他试剂任选,写出合成吸水材料聚丙烯酸钠的合成路线___________________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于100mL1mol/L盐酸与铁片的反应,采取下列措施,其中不能使反应速率加快的是( )
A.升高温度
B.改用50mL2mol/L盐酸
C.改用200mL1mol/L盐酸
D.用等量铁粉代替铁片
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是重要的有机化工原料。下列关于乙烯的有关说法不正确的是( )
A.一种植物生长调节剂B.易燃
C.能使溴水、酸性高锰酸钾溶液褪色D.与甲烷互为同系物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com