
| A. | 第一电离能大小:S>P>Si | |
| B. | 电负性顺序:C<N<O<F | |
| C. | 晶格能是气态离子形成1摩离子晶体释放的能量,晶格能越大,形成的离子晶体越稳定 | |
| D. | 由于N2和O22+互为等电子体,所以可以推断O22+的电子式为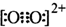 |
分析 A.P原子核外最外层原子轨道为半充满状态,第一电离能大于相邻元素;
B.同周期元素从左到右,电负性逐渐增强;
C.离子晶体的晶格能越大,晶体的熔点越高,越稳定;
D.等电子体具有相似的结构和性质.
解答 解:A.P原子核外最外层原子轨道为半充满状态,第一电离能大于相邻元素,应为P>S,故A错误;
B.同周期元素从左到右,电负性逐渐增强,故B正确;
C.离子晶体的晶格能越大,离子键越难以断裂,则形成的离子晶体越稳定,故C正确;
D.等电子体具有相似的结构和性质,氮气中存在N≡N键,则O22+存在O≡O键,电子式为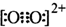 ,故D正确.
,故D正确.
故选A.
点评 本题考查较为综合,涉及电荷性、第一电离能、晶体的熔沸点比较、等电子体等知识,为高频考点,侧重于学生的分析能力的考查,注意相关基础知识的积累,难度不大.


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:选择题
| A. | 乙醇中的水:CaO,蒸馏 | B. | 乙酸乙酯中的乙酸:NaOH溶液,分液 | ||
| C. | 乙醇中的苯酚:溴水,过滤 | D. | 乙烷中的乙烯:溴水,分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实验目的 | 实验操作 | |
| A. | 验证乙炔能被酸性高锰酸钾溶液氧化 | 将电石与饱和食盐水反应生成的气体通入酸性高锰酸钾溶液,观察溶液是否褪色 |
| B. | 检验淀粉水解产物的还原性 | 取少量淀粉溶液,与稀硫酸共热后再加入银氨溶液,水浴加热,观察是否出现银镜 |
| C. | 除去乙酸乙酯中混有的少量乙酸 | 加入足量饱和NaHCO3溶液,振荡,静置,分液,取出上层液体 |
| D. | 检验溴乙烷中的溴元素 | 取少量溴乙烷,与氢氧化钠溶液共热后加入硝酸银溶液,观察是否出现白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 物质及变化 | 描述 | 相关知识 | |
| A | 瓦斯 | 混合物 | 主要成分为CO、H2 |
| B | 煤的干馏 | 物理变化 | 主要产品为焦炉气、煤焦油、粗氨水和焦炭 |
| C | 水煤气 | 混合物 | 一种高效的燃料 |
| D | 淀粉和纤维素 | 多糖 | 二者互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知C-C键可以绕键轴自由旋转,结构简式为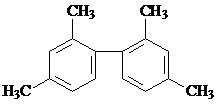 分子中至少有11个碳原子处于同一平面上 分子中至少有11个碳原子处于同一平面上 | |
| B. | 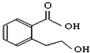 能发生的反应类型有:加成反应、取代反应、消去反应、酯化反应、水解反应 能发生的反应类型有:加成反应、取代反应、消去反应、酯化反应、水解反应 | |
| C. | 3-甲基-3-乙基戊烷的一氯取代产物为5种 | |
| D. | 相同条件下乙酸乙酯在水中的溶解度比在乙醇中的溶解度要大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
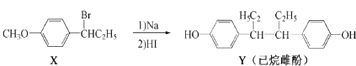
| A. | 在NaOH水溶液中加热,化合物X可发生消去反应 | |
| B. | 化合物Y不能与HCHO发生反应 | |
| C. | 用FeCl3溶液可鉴别化合物X和Y | |
| D. | 化合物Y中共含有四种氢原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1-丁烯、2-丁烯都存在顺反异构 | |
| B. | 乙二醇和丙三醇为同系物 | |
| C. | 正戊烷、异戊烷、新戊烷的沸点逐渐降低 | |
| D. | 淀粉、纤维、脂肪、蛋白质都是天然高分子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com