
| A. |  探究乙烯与Br2的加成反应 | B. | 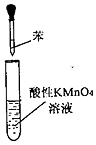 探究苯分子是否含有碳碳双键 | ||
| C. | 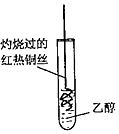 探究乙醇的还原性 | D. | 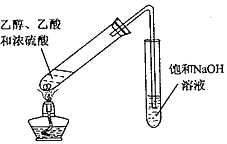 制取少量乙酸乙酯 |
分析 A.HBr不溶于四氯化碳,根据溶液表明是否有气泡生成可判断乙烯与溴的反应类型;
B.碳碳双键能够使酸性高锰酸钾溶液褪色;
C.乙醇能够使灼热的铜丝变为红色,证明乙醇还原了氧化铜;
D.氢氧化钠溶液能够与乙酸乙酯反应,不能用氢氧化钠吸收乙酸乙酯.
解答 解:A.乙烯与溴发生加成反应生成1,2-二溴乙烷,若发生取代反应生成溴乙烷和HBr,由于HBr不溶于四氯化碳,可根据四氯化碳溶液避免是否有气泡生成判断反应类型,故A正确;
B.酸性高锰酸钾溶液能够氧化碳碳双键,根据图示装置可探究苯分子是否含有碳碳双键,故B正确;
C.灼热的铜丝表明有黑色的CuO,将灼热的铜丝伸入乙醇中,黑色的氧化铜变为红色,可证明乙醇具有还原性,故C正确;
D.乙酸乙酯与氢氧化钠溶液反应,应该用饱和碳酸钠溶液吸收乙酸乙酯,故D错误;
故选D.
点评 本题考查化学实验方案的评价,题目难度不大,涉及反应类型判断、乙酸乙酯的制备、乙醇的性质、物质检验等知识,明确常见有机物组成、结构与性质为解答关键,试题培养了学生的分析能力及综合应用能力.


 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:选择题
| X | Y | ||
| Z | W |
| A. | 气态氢化物的热稳定性:X<Y | |
| B. | 最高价氧化物对应水化物的酸性:W>Z>X | |
| C. | X、Y元素均存在同素异形体 | |
| D. | W的单质具有漂白性,能使干燥的有色布条褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2、I2(g)、HI平衡混合气体加压后颜色变深(已知:H2+I2?2HI) | |
| B. | 棕红色的NO2加压后颜色先变深后变浅(已知:2NO2 (g)?N2O4 (g)) | |
| C. | 工业上生产硫酸的过程中,使用过量的空气以提高SO2的利用率 | |
| D. | 滴加酚酞的氨水中加入氯化铵固体后红色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3 | B. | 2 | C. | 5 | D. | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某浓度的硫酸中投入2.5g在空气中久置的铝片,该铝片与硫酸反应产生氢气的速率v与反应时间t可用如图来表示,下列叙述不正确的是( )
某浓度的硫酸中投入2.5g在空气中久置的铝片,该铝片与硫酸反应产生氢气的速率v与反应时间t可用如图来表示,下列叙述不正确的是( )| A. | O→a不产生氢气是因为氧化铝和硫酸反应 | |
| B. | b→c产生氢气的速率增大较快的主要原因之一是温度升高 | |
| C. | t=c时反应处于平衡状态 | |
| D. | t>c产生氢气的速率减小主要是因为溶液中的c(H+)降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数为10的氧原子:${\;}_{18}^{10}$O | B. | Na2S的电子式: | ||
| C. | 乙酸的球棍模型: | D. | 葡萄糖的结构简式:C6H12O6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com