
氢气和氟气混合在黑暗处即可发生爆炸而释放出大量的热量。在反应过程中,断裂1molH2中的化学键消耗的能量为Q1kJ,断裂1molF2中的化学键消耗的能量为Q2kJ,形成1molHF中的化学键释放的能量为Q3kJ。下列关系式中正确的是
A.Q1+ Q2<2Q3 B.Q1+ Q2>2Q3 C.Q1+ Q2<Q3 D.Q1+ Q2>Q3
A
【解析】
试题分析:断裂1molH2中的化学键消耗的能量为Q1kJ,则H-H键能为Q1kJ/mol,断裂1molF2中的化学键消耗的能量为Q2kJ,则F-F键能为Q2kJ/mol,形成1molHF中的化学键释放的能量为Q3kJ,则H-F键能为Q3kJ/mol,对于H2(g)+F2(g)=2HF(g)
反应热△H=反应物的总键能-生成物的总键能=Q1kJ/mol+Q2kJ/mol-2Q3kJ/mol=(Q1+Q2-2Q3)KJ/mol.
由于氢气和氟气混合在黑暗处即可发生爆炸而释放出大量的热量,反应热△H<0,即(Q1+Q2-2Q3)<0,所以Q1+Q2<2Q3,答案选A。
考点:考查反应热与键能的关系


科目:高中化学 来源:2013-2014重庆一中高一下学期期末考试化学试卷(解析版) 题型:选择题
(原创)科学家发现海洋是一个名副其实的“聚宝盆”,一些国家觊觎我国南海海域的丰富资源,导致近年来南海争端不断。下列对海洋资源开发利用的说法不正确的是
A.海底如“土豆”般的金属结核矿含有铁、锰、钴等多种元素,可用铝热法冶炼并分离得到各种金属单质
B.海水淡化工厂可与化工生产结合,如淡化后的浓海水,可用于提溴、镁、钠等
C.海水中的金、铀等元素储量高、浓度低,提炼时,须先富集
D.海水提镁过程中,所需的石灰乳,可用贝壳煅烧后加水得到,体现了就地取材、降低成本的生产理念
查看答案和解析>>
科目:高中化学 来源:2013-2014辽宁省高三仿真测试理科综合化学试卷(解析版) 题型:填空题
对某芳香烃A分析结果如下:质谱图显示其最大质荷比为120,红外光谱显示其有两个甲基,核磁共振氢谱显示有五种峰且其面积比为1:2:2:1:6,A在有机合成中能发生如下转化:

(已知:烃基发生取代反应的活性次序为 CH > CH2 > CH3 即叔氢>仲氢>伯氢)
回答以下问题:
(1)写出A的结构简式 ;
(2) 反应①和②相同的反应试剂和条件为 ;
(3)F分子中的含氧官能团名称是 ;
(4)反应③的化学方程式为: ;
(5)写出满足下列条件的H分子的所有同分异构体的结构简式:
①含有苯环 ②1 mol有机物发生银镜反应生成4 mol Ag ③苯环上的一溴代物有两种
;
(6)与H具有相同官能团的H的同分异构体有四种,其中一种分子K还存在顺反异构
体,试写出K的结构简式: 。
查看答案和解析>>
科目:高中化学 来源:2013-2014辽宁省五校第二学期期末联考高一化学试卷(解析版) 题型:填空题
(6分)苹果酸结构如下,常用做汽水、糖果的添加剂。

试写出苹果酸分别与下列物质反应的化学方程式:
(1)与Na 。
(2)与Na2CO3 __________________________。
(3)与CH3CH2OH按物质的量比1∶2反应(浓H2SO4,△)_________ __ 。
查看答案和解析>>
科目:高中化学 来源:2013-2014辽宁省五校第二学期期末联考高一化学试卷(解析版) 题型:选择题
下列用水就能鉴别的一组物质是
A.苯、己烷、四氯化碳 B.苯、乙醇、四氯化碳
C.硝基苯、乙醇、四氯化碳 D.硝基苯、乙醇、乙酸
查看答案和解析>>
科目:高中化学 来源:2013-2014福建龙岩市毕业联合考试理综化学试卷(解析版) 题型:填空题
(16分)辉铜矿是冶炼铜的重要原料。
(1)工业上冶炼粗铜的某种反应为:Cu2S+O2=2Cu+SO2
①当产生标况下11.2L气体时,转移电子数目为 ;
②将粗铜进行电解精炼,粗铜应与外电源的 极相接;若精炼某种仅含杂质锌的粗铜,通电一段时间后测得阴极增重ag,电解质溶液增重bg,则粗铜中含锌的质量分数为 ;
(2)将辉铜矿、软锰矿做如下处理,可以制得碱式碳酸铜:
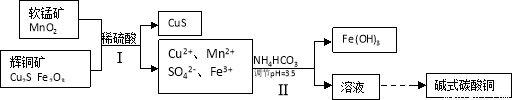
①铜单质放置于潮湿空气中,容易生成碱式碳酸铜,反应化学方程式是 ;
②步骤Ⅱ中,碳酸氢铵参与反应的离子方程式为 ;
③步骤Ⅰ中发生如下3个反应,已知反应i)中生成的硫酸铁起催化作用。请写出反应iii)的化学方程式。
i)Fe2O3+3H2SO4 =Fe2(SO4)3+3H2O
ii) Cu2S+ Fe2(SO4)3 =CuSO4+CuS+2FeSO4
iii)
④步骤Ⅱ中调节pH后的溶液中,铜离子浓度最大不能超过 mol/L。
(已知Ksp[(Cu(OH)2)]=2×10-a)
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高三高考模拟理综化学试卷(解析版) 题型:选择题
下列陈述中,Ⅰ、Ⅱ都正确且两者间具有因果关系的一组是
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | FeCl3溶液能腐蚀Cu | Fe的金属性强于Cu |
B | Na2O2使酚酞溶液变红 | Na2O2是碱性氧化物 |
C | Cl2可部分与水反应 | 用排饱和食盐水法收集Cl2 |
D | 浓H2SO4可干燥NO和SO2 | NO和SO2还原性都弱 |
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县第二学期期中考试高一化学试卷(解析版) 题型:实验题
用图1所示的Ⅰ和Ⅱ装置组合与Ⅰ和Ⅲ装置组合可以进行相关实验(夹持仪器省略),回答下列问题:

(1)若用Ⅰ和Ⅱ装置或Ⅰ和Ⅲ装置组合,实验前须检验 。
(2)在Ⅰ和Ⅱ装置组合中,若a为浓硫酸,b为铜粉,c容器中盛放品红溶液,旋开f后,给烧瓶加热,一段时间后c中的现象是 写出烧瓶中发生反应的化学方程式
(3)在Ⅰ装置中,若a为浓氨水,b为生石灰,欲制取氨气并证明氨水有碱性,最好应选用 (填“Ⅱ”或“Ⅲ”)装置与其组合,原因是
(4)在Ⅰ装置中,若a为可能含有Mg2+、Cu2+、Al3+、Fe3+四种阳离子的水溶液,b为过氧化钠固体,旋开f后,有白色沉淀产生并放出氧气,过氧化钠固体的物质的量与产生沉淀的质量关系如图2,则a溶液中含有的阳离子有 。(写化学式)
(5)在图2中A→B段反应过程中溶液所增加的阴离子是 (写化学式)

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com