
| △ |
| 水 |
| △ |
| 水 |
 CH3COOC2H5+H2O;
CH3COOC2H5+H2O; CH3COOC2H5+H2O;
CH3COOC2H5+H2O;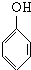 +nHCHO
+nHCHO 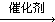
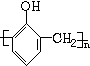 +nH2O,
+nH2O, +nHCHO
+nHCHO 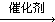
 +nH2O.
+nH2O.


 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:
A、.已知
| ||||||||||||||||||||||||||
| B、已知:25℃时,CaCO3的Ksp为2.9×10-9,CaF2的Ksp为2.7×10-11在CaCO3悬浊液中加入NaF固体,CaCO3不可能全转化为CaF2 | ||||||||||||||||||||||||||
C、常温下
| ||||||||||||||||||||||||||
D、由下列短周期元素性质的数据推断元素⑤最高价氧化物对应的水化物酸性最强
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol H2O的质量为18g/mol |
| B、3.01×1023个SO2分子的质量为32g |
| C、CH4的摩尔质量为16g |
| D、标准状况下,1 mol任何物质的体积均为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子晶体中只含有共价键 |
| B、离子晶体中只含有离子键,不含有共价键 |
| C、分子晶体中只存在分子间作用力,不含有其他化学键 |
| D、任何晶体中,若含有阳离子也一定含有阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子化合物中只存在阴、阳离子之间的静电作用 |
| B、相同质量的N2、N4、N30含有的分子数相同 |
| C、23g钠和足量水反应失去6.02×1023个电子 |
| D、当1molCl2的体积为22.4L时,该氯气一定处于标准状况下 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 某兴趣小组设计如图实验装置进行实验.
某兴趣小组设计如图实验装置进行实验.
| 实验操作 | 预期现象与结论 |
| 步骤1:取适量“吸收液”于小烧杯中,用胶头滴管取l mol/L BaCl2溶液向小烧杯滴加直至过量. | 若出现白色浑浊, 则“吸收液”中存在SO32-或 SO42-. |
| 步骤2:将小烧杯中的浊液过滤、洗涤,再用适量水把附在滤纸上的固体冲入另一小烧杯中;向冲下的固体 | 则“吸收液”中存在 SO32-. |
| 步骤3: | 则“吸收液”中存在 HSO3-. |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com