
| A. | 溶液中c(H+)>c(OH-) | |
| B. | NH4+水解是微弱的 | |
| C. | NH3•H2O是弱碱 | |
| D. | 由H2O电离出的c(H+)<10-7 mol/L | |
| E. | 物质的量浓度相等的氨水和盐酸等体积混合,溶液pH=7 |
分析 室温下,使用pH计测定0.1mol/L NH4Cl溶液的pH=5.12,说明氯化铵水解呈酸性,为强酸弱碱盐,则NH3•H2O是弱碱,以此解答该题.
解答 解:溶液的pH=5.12,呈酸性.
A.溶液呈酸性,c(H+)>c(OH-),故A正确;
B.pH=5.12,溶液呈弱酸性,则NH4+水解是微弱的,故B正确;
C.氯化铵水解呈酸性,为强酸弱碱盐,则NH3•H2O是弱碱,故C正确;
D.盐类水解促进电离,则由H2O电离出的c(H+)>10-7 mol/L,故D错误;
E.物质的量浓度相等的氨水和盐酸等体积混合,恰好生成氯化铵,发生水解,溶液呈酸性,故D错误.
故选ABC.
点评 本题考查弱电解质的电离,为高频考点,侧重考查学生的分析能力,注意把握弱电解质的电离以及盐类水解的特点,把握水的电离平衡的影响因素,难度不大.


科目:高中化学 来源: 题型:推断题
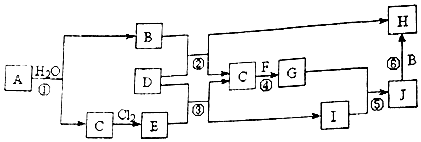
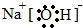 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时,Co元素的化合价升高 | |
| B. | 放电时,正极的电极反应式为Lil-xCoO2+xe-+xLi+=LiCoO2 | |
| C. | 充电时,Li+在电解质中由阳极向阴极迁移 | |
| D. | 充电时,阴极的电极反应式为C6+xLi++xe-=LixC6 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×l0-10 |
| CH3COOH | K=1.8×l0-5 |
| H2CO3 | K1=4.3×l0-7、K2=5.6×l0-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
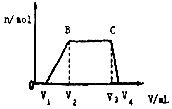 1L某混合溶液,可能含有的离子如表:
1L某混合溶液,可能含有的离子如表:| 可能大量含有的阳离子 | H+、K+、Mg2+、Al3+、NH4+、Fe2+、Fe3+ |
| 可能大量含有的阴离子 | Cl-、Br-、I-、CO32-、AlO2- |
| Cl2的体积(标准状况) | 2.8L | 5.6L | 11.2L |
| n(Cl-) | 1.25mol | 1.5mol | 2mol |
| n(Br-) | 1.5mol | 1.4mol | 0.9mol |
| N(I-) | a mol | 0 | 0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com