
NA为阿伏加德罗常数,下列叙述错误的是
A.18gH2O中含有的质子数为10NA
B.常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2NA
C.46g NO2和N2O4混合气体中含有原子总数为3NA
D.1molNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
科目:高中化学 来源:2015-2016学年江苏省高二上第二次质检化学试卷(解析版) 题型:填空题
A.《化学与生活》
(1)材料是经济和生态文明建设的重要物资基础
①生产硅酸盐水泥和普通玻璃都需用到的共同原料是________。
②橡胶是制造轮胎的重要原料,橡胶属于_______ (填字母)
A.金属材料 B.无机非金属材料 C.有机高分子材料
③钢铁制品在潮湿的空气中能发生_______腐蚀,发生该腐蚀时的负极电极反应式为________。
(2)防冶环境污染,改善生态环境已成为全球共识
①2013年,全国多个省市出现严重的雾天气,导致雾形成的主要污染物是_____(填字母)
A.O2 B.CO2 C.PM2.5
②采用焚烧处理垃圾进行发电已在江苏投入使用。下列是生活中的常见垃圾;
A.废电池 B.易拉罐 C.玻璃瓶
在焚烧前,除废电池外,还有_______(填字母)应剔除并回收,随意丢弃电池造成的主要危害是_______。
③漂白粉可用于生活用水的杀菌消毒,工业上利用氯气和石灰乳制取漂白粉的化学方程式是_______。
(3)合理膳食,保持营养均衡,是青少年学生健康成长的重要保证。
①维生素C能增强人体对疾病的抵抗能力,促进人体生长发育,中学生每天要补充60mg的维生素C;下列物质含有丰富维生素C的是______(填字母)
A.牛肉 B.辣椒 C.鸡蛋
②青少年及成人缺乏某种微量元素将导致甲状腺肿大,而且会造成智力损害,该微量元素是______(填字母)A.碘 B.铁 C.钙
③蛋白质是人体必需的营养物质,它在人体内最终水解为___________。
(4)(3分)材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活。
①居室装修所使的人造板材会释放出一种挥发性物质,长期接触会引起过敏性皮炎,免疫功能异常,该挥发性物质是_________。
②玻璃是重要的硅酸盐产品,生产玻璃时,石灰石与石英反应的化学方程式为___________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古赤峰二中高二上第二次月考化学试卷(解析版) 题型:推断题
化合物F是一种抗心肌缺血药物的中间体,可以通过以下方法合成:

(1)化合物A中的含氧官能团为 和 (填官能团名称)。
(2)化合物B的结构简式为 ;由C→D的反应类型是 。
(3)写出同时满足下列条件的E的所有同分异构体的结构简式 。
Ⅰ.分子中含有2个苯环
Ⅱ.分子中含有3种不同化学环境的氢
(4)已知:RCH2CN RCH2CH2NH2,请写出以
RCH2CH2NH2,请写出以 为原料制备化合物X(结构简式见下图)的合成路线流程图(无机试剂可任选)。
为原料制备化合物X(结构简式见下图)的合成路线流程图(无机试剂可任选)。

合成路线流程图示例如下:
CH3CHO CH3COOH
CH3COOH CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一12月月考化学试卷(解析版) 题型:选择题
铁和氧化铁的混合物共amol,加盐酸后固体全部溶解,共收集到2bgH2,且溶液中加入KSCN溶液不显红色,则原混合物中铁的物质的量为
A.b mol B.(a-b)mol C.1/2(a?b)mol D.1/2(a+b)mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二上12月月考化学试卷(解析版) 题型:选择题
下列叙述Ⅰ和Ⅱ均正确并有因果关系的是
选项 | 叙述Ⅰ | 叙述Ⅱ |
A | 乙二酸可与KMnO4溶液发生反应 | 乙二酸具有酸性 |
B | 向氯化钙溶液中通入足量的CO2有 白色沉淀生成 | CaCO3不溶于水 |
C | 1-己醇的沸点比己烷的沸点高 | 1-己醇和己烷可通过蒸馏初步分离 |
D | Na在Cl2中燃烧的生成物含离子键 | NaCl固体可导电 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二上期中测试化学试卷(解析版) 题型:填空题
【加试题】节能减排已经成为全社会的共识,浙江省在原先推行乙醇汽油的基础上,开始试点甲醇汽油(即在汽油中添加一定量的甲醇),根据检测的数据分析认为,若绍兴全市的100余万辆机动车全部使用甲醇汽油,一年内能减少有害气体(一氧化碳)排放将近100万吨。甲醇常利用煤气化过程中生成的CO和H2来制备:CO+2H2?CH3OH 。
请根据图示回答下列:

(1)关于该自发反应的下列说法中,正确的是 (填字母):
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)现进行如下实验,在体积为1L的密闭容器中,充入1molCO和3molH2,测得CO和CH3OH(g)的浓度随时间变化如图所示。从反应开始到平衡,CO的平均反应速率v(CO)= mol/(L•min),该反应的平衡常数K= 。
(3)恒容条件下,达到平衡后,下列措施中能使n(CH3OH)/n(CO)增大的有 。
A.升高温度 B.充入He气 C.再冲入1molCO和3molH2 D.使用催化剂
(4)若在一体积可变的密闭容器中充入1molCO、2molH2和1molCH3OH,达到平衡时测的混合气体的密度是同温同压下起始的1.6倍(此过程三种物质均处于气态),则平衡时混合气体的平均摩尔质量= g/mol。
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上一轮收官考试理综化学试卷(解析版) 题型:选择题
NA代表阿伏加德罗常数的值,下列有关叙述不正确的是( )
A.在熔融状态下,1molNa2O2完全电离出的离子数目为3NA
B.将CO2通过Na2O2使固体质量增加mg,反应中转移的电子数m NA /14
C.在标准状况下,22.4LCH4与18 gH2O所含有的电子数均为10NA
D.含1mol Cl-的NH4Cl溶液中加入适量氨水使溶液呈中性,此时溶液中NH4+数为 NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东汕头金山中学高二上10月月考化学卷(解析版) 题型:填空题
(1)近年来,我国储氢纳米碳管研究取得重大进展,用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法提纯,其反应化学方程式为:
C+ K2Cr2O7+ H2SO4 ═ CO2↑+ K2SO4+ Cr2(SO4)3+ H2O
请完成并配平上述化学方程式.其中氧化剂是 ,氧化产物是
(2)甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产.工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
CO(g)+2H2(g)?CH3OH(g) △H1=﹣116kJ•mol﹣1
①已知:2CO(g)+O2(g)=2CO2(g) △H2=﹣566kJ•mol﹣1
2H2(g)+O2(g)=2H2O(g) △H3=﹣484kJ•mol﹣1
则表示1mol气态甲醇完全燃烧生成CO2和水蒸气时的热化学方程式为 ;
②在容积为1L的恒容容器中,分别研究在230℃、250℃、270℃三种温度下合成甲醇的规律.如图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系.请回答:
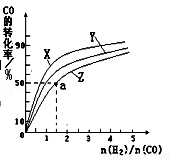
A)在上述三种温度中,曲线Z对应的温度是
B)利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+2H2(g)?CH3OH(g)的平衡常数K= .(写明单位)
③在某温度下,将一定量的CO和H2投入10L的密闭容器中,5min时达到平衡,各物质的物质的浓度(mol•L﹣1)变化如下表所示:
0min | 5min | 10min | |
CO | 0.1 | 0.05 | |
H2 | 0.2 | 0.2 | |
CH3OH | 0 | 0.04 | 0.05 |
若5min~10min只改变了某一条件,所改变的条件是 ;且该条件所改变的量是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com