
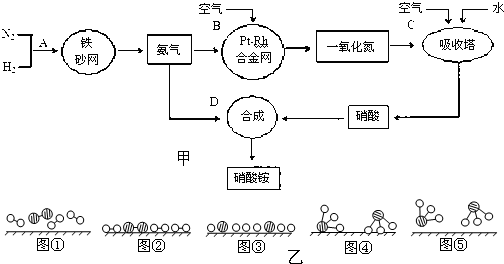
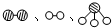 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是______、______.
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是______、______.
| ||
| △ |
| 注意事项 | 理由 | |
| ① | ||
| ② |
| ||
| △ |
| 1mol |
| 1mol+0.8832mol |
| ||


 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案科目:高中化学 来源:不详 题型:填空题
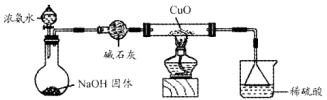
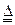 N2+3Cu+3H2O。
N2+3Cu+3H2O。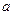 mol气体后,烧杯中的溶液能使酚酞变红。试依据“化学实验设计基本要求”设计制备硫酸亚铁铵溶液的方案,清简述实验方法。
mol气体后,烧杯中的溶液能使酚酞变红。试依据“化学实验设计基本要求”设计制备硫酸亚铁铵溶液的方案,清简述实验方法。 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.分别加热溶液,有紫红色蒸汽产生的是KI溶液 |
| B.分别加入淀粉,便蓝色的是KI溶液 |
| C.分别加入四氯化碳振荡,静置后下层呈紫红色的是KI溶液 |
| D.分别加入氯水、四氯化碳振荡,静置后下层呈紫红色的是KI溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②④ | B.①②⑤ | C.②③④ | D.②④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
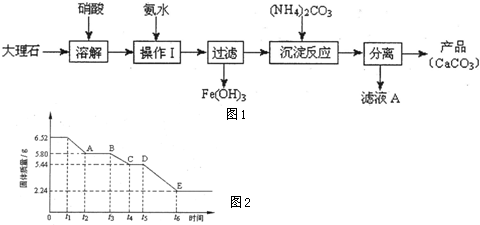
| ||
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

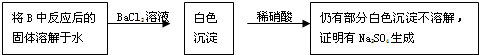
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com