
| A. | 1:6 | B. | 2:15 | C. | 2:11 | D. | 1:7 |
分析 根据FeS化学式可知,溶液中铁离子与硫酸根离子的物质的量相等,设参加反应的FeS为1mol,则溶液中Fe2(SO4)3为$\frac{1}{3}$mol,Fe(NO3)3为$\frac{1}{3}$mol,反应中Fe元素、S元素化合价升高,N元素化合价降低,根据电子转移守恒计算NO2、N2O4、NO各的物质的量,进而计算起氧化剂作用的HNO3,参加反应的硝酸为起氧化剂作用的硝酸与起酸作用的硝酸之和,据此计算.
解答 解:令参加反应的FeS为1mol,则溶液中Fe2(SO4)3为$\frac{1}{3}$mol,Fe(NO3)3为$\frac{1}{3}$mol,
反应中Fe元素、S元素化合价升高,N元素化合价降低,设NO2、N2O4、NO的物质的量分别为amol、amol、amol,
根据电子转移守恒可得:1×(3-2)+1×[6-(-2)]=a×(5-4)+a×(5-4)×2+a×(5-2),解得:a=1.5,
所以NO2、N2O4、NO的物质的量分别为1.5mol、1.5mol、1.5mol,则起氧化剂作用的HNO3为:1.5mol+1.5mol×2+1.5mol=6mol,起酸的作用的硝酸生成Fe(NO3)3,则起酸的作用的硝酸为:$\frac{1}{3}$mol×3=1mol,参加反应的硝酸为6mol+1mol=7mol,
所以实际参加反应的FeS与HNO3的物质的量之比为:1mol:7mol=1:7,
故选D.
点评 本题考查氧化还原反应有关计算,题目难度中等,利用电子转移守恒与元素守恒计算是关键,转移守恒思想在氧化还原反应计算中的运用,试题培养了学生的化学计算能力.


 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制氯水中只含Cl2和H2O 分子 | |
| B. | 新制氯水可使蓝色石蕊试纸变红且不褪色 | |
| C. | 光照氯水有气泡逸出,该气体是Cl2 | |
| D. | 氯水放置数天后酸性将变强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 将等体积、等物质的量浓度的CH3COONH4与CH3COONa溶液混合:c(CH3COO-)>c(Na+)>c(NH4+)>c(OH-) | |
| B. | 将等体积、等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体后的溶液:c(H+)+c(H2CO3)=c(OH-)+c(CO32-)+c(NH3•H2O) | |
| C. | 向饱和氯水中加入NaOH溶液至pH=7,所得溶液中:c(Na+)>c(ClO-)>c(Cl-)>c(OH-) | |
| D. | 向0.10mol•L-1 Na2CO3溶液中通入少量CO2的溶液中:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ②④ | C. | ①③ | D. | ① |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
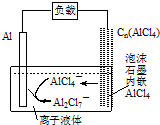 最近中美研究人员发明了一种可快速充放电的铝离子电池,该电池电解质为离子液体{AlCl3/[EMIM]Cl},放电时有关离子转化如图所示.下列说法正确的是( )
最近中美研究人员发明了一种可快速充放电的铝离子电池,该电池电解质为离子液体{AlCl3/[EMIM]Cl},放电时有关离子转化如图所示.下列说法正确的是( )| A. | 放电时,负极发生:2AlCl4--e-=Al2Cl7-+Cl- | |
| B. | 放电时,电路中每流过3mol电子,正极减少27g | |
| C. | 充电时,泡沫石墨极与外电源的负极相连 | |
| D. | 充电时,阴极发生:4Al2Cl7-+3e-=Al+7AlCl4- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com