
下列变化属于物理变化的是 ( )
A.氧气在放电条件下变成臭氧
B.胆矾在加热条件下变成白色无水硫酸铜
C.漂白的草帽久置空气中变黄
D.氢氧化铁胶体加入硫酸镁产生沉淀
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源:2013-2014黑龙江省高二下学期期末考试化学试卷(解析版) 题型:实验题
(10分)某研究性学习小组的同学利用下列装置进行乙醇催化氧化的实验。请分析回答:

(1)请写出实验过程中的总的化学反应方程式______________________________。
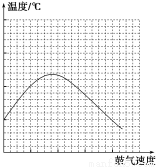
(2)在不断鼓入空气的情况下,移去酒精灯,反应仍能继续进行,说明乙醇的催化氧化反应是________反应。进一步研究表明,鼓气速度与反应体系的温度关系曲线如右图所示。鼓气速度过快,反应体系温度反而下降的原因___________________________。
(3)甲和乙两个水浴作用不相同。
甲的作用是________________;乙的作用是_________________________。
(4)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是___________。集气瓶中收集到的气体的主要成分是_______________。
(5)在检验生成物的过程中,一位同学很偶然地发现向溴水中加入乙醛溶液,溴水褪色。针对溴水褪色的原因,该小组的同学们经过分析后,提出两种猜想:
①溴水将乙醛氧化为乙酸;②溴水与乙醛发生加成反应。
请你设计一个简单的实验,探究哪一种猜想正确?__________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高一下学期期末考试化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数的值。下列叙述中不正确的是( )
A.1mol乙烯与乙醇的混合物在氧气中充分燃烧,消耗氧气的分子数为一定为3NA
B.28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA
C.常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
D.常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2 NA
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高二下学期期末考试化学试卷(解析版) 题型:选择题
下列关于Na2O2的叙述,正确的是 ( )
A.Na2O2晶体中的阴离子与阳离子的物质的量之比为1:1
B.Na2O2晶体为离子晶体,且含极性共价键
C.Na2O2应保存于密封、干燥带玻璃塞的广口瓶中
D.Na2O2与盐酸反应,不仅有盐和水生成,同时会放出无色气体
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高二下学期期末考试化学试卷(解析版) 题型:选择题
下列各组离子或分子在溶液中能大量共存,且满足相应要求的是 (. )
选项 | 离子或分子 | 要求 |
A | K+ 、NO3-、Cl-、HS- | c(K+)<c(Cl-) |
B | Fe3+、NO3-、SO32-、Cl- | 滴加盐酸立即有气体产生 |
C | NH4+、Al3+、SO42-、CH3COOH | 滴加NaOH溶液立即有气体产生 |
D | Na+、HCO3-、Mg2+、SO42- | 逐滴滴加氨水立即有沉淀产生 |
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高一下学期期末考试化学试卷(解析版) 题型:填空题
(10分)Ⅰ 乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请回答下列问题。(1)乙烯的电子式____________,结构简式____________。
(2)鉴别甲烷和乙烯的试剂是______(填序号)。
A.稀硫酸B.溴的四氯化碳溶液 C.水D.酸性高锰酸钾溶液
(3)下列物质中,可以通过乙烯加成反应得到的是______(填序号)。
A.CH3CH3B.CH3CHCl2
Ⅱ 红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯。在实验室也可以用如下图所示的装置制取乙酸乙酯,请回答下列问题。
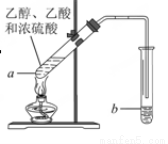
(1)乙醇分子官能团名称是__________________。
(2)试管a中加入几块碎瓷片的目的是____________。
(3)试管a中发生反应的化学方程式为___________,反应类型是________________________。
(4)反应开始前,试管b中盛放的溶液是____________。作用是 。
(5)可用____________的方法把制得的乙酸乙酯分离出来。
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高一下学期期末考试化学试卷(解析版) 题型:选择题
下面关于化学反应的限度的叙述中,正确的是
A.化学反应的限度都相同
B.可以通过改变温度控制化学反应的限度
C.可以通过延长化学反应的时间改变化学反应的限度
D.当一个化学反应在一定条件下达到限度时,反应即停止
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高一下学期期末考试化学试卷(解析版) 题型:选择题
根据下列各反应现象所归纳的元素性质不正确的是
A.将一小块钠投入到盛有硫酸铜溶液的烧杯中,发现没有紫红色的铜析出。不能说明钠的金属性比铜弱
B.用湿润的淀粉碘化钾试纸放置在有氯气产生的导管上端,发现试纸变蓝。说明氯元素的非金属性比碘元素强
C.把H2S气体和Cl2在集气瓶中混合,一段时间后发现瓶壁有淡黄色固体析出。说明Cl的非金属性比S强
D.将0.1 mol Na、Mg、Al分别与足量稀盐酸反应,除共同产生H2外,还分别生成了NaCl、MgCl2、AlCl3,金属失去的电子数分别为0.1 mol、0.2 mol、0.3 mol。说明这三种金属的活泼性为:Al>Mg>Na
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高一下学期期中考试化学试卷(解析版) 题型:选择题
下列变化为放热的化学反应的是

A.H2O(g)===H2O(l) ΔH=-44.0 kJ·mol-1
B.2HI(g)===H2(g)+I2(g)
ΔH=+14.9 kJ·mol-1
C.形成化学键时共放出862 kJ能量的化学反应
D.能量变化如右图所示的化学反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com