(2007?德阳模拟)某学生用如图所示的装置制取氯气,并收集氯气进行实验.请回答下列问题:
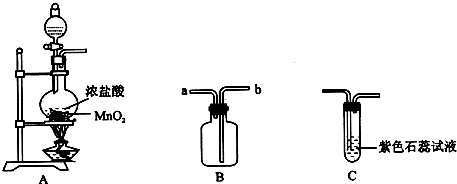
(1)装置 A 中发生反应的化学方程式为
MnO
2+4HCl(浓)
MnCl
2+Cl
2↑+2H
2O
MnO
2+4HCl(浓)
MnCl
2+Cl
2↑+2H
2O
.
(2)装置 B 中连接 A 的接口是
b
b
(填 B 中的接口编号).
(3)实验中 C 处可观察到的现象是
石蕊试液先变化后褪色
石蕊试液先变化后褪色
.
(4)将 B 中收集到的氯气与铜丝进行实验.其操作是先把铜丝在酒精灯火焰上灼热,然后立即放入充满氯气的集气瓶中.该项实验不需在集气瓶底部放入少量的水或细沙的理由是
因为铜与氯气反应生成的产物是烟不是高温熔融物,不会造成瓶底炸裂
因为铜与氯气反应生成的产物是烟不是高温熔融物,不会造成瓶底炸裂
(5)实验表明,用高锰酸钾和浓盐酸在室温下就能很快放出氯气,由此说明在二氧化锰和高锰酸钾中氧化性较强的是
KMnO4
KMnO4
(填物质的化学式).




 阅读快车系列答案
阅读快车系列答案