
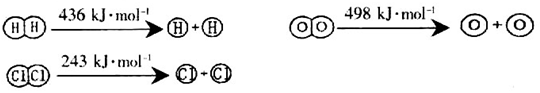
 ,它所对应的化学方程式为________________。
,它所对应的化学方程式为________________。 2NH3(g) △H<0在400℃时K=0.5,此条件下在0.5L的密闭容器中进行该反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应υ(N2)正______υ(N2)逆(填“>”、“<”或“=”)。欲使得该反应的化学反应速率加快,同时使平衡时NH3的体积百分数增加,可采取的措施是_______(填序号)。
2NH3(g) △H<0在400℃时K=0.5,此条件下在0.5L的密闭容器中进行该反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应υ(N2)正______υ(N2)逆(填“>”、“<”或“=”)。欲使得该反应的化学反应速率加快,同时使平衡时NH3的体积百分数增加,可采取的措施是_______(填序号)。 2C(g)+D(s) △H,其化学平衡常数K与T的关系如下表:
2C(g)+D(s) △H,其化学平衡常数K与T的关系如下表:| T/K | 300 | 400 | 500 | …… |
| K/(mol·L-1)2 | 4×106 | 8×107 | 1.2×109 | …… |
 CO(g)+H2(g)(1分,不标状态不扣分,写成等号不给分)
CO(g)+H2(g)(1分,不标状态不扣分,写成等号不给分) 可知,该反应的方程式为C(s)+H2O(g)
可知,该反应的方程式为C(s)+H2O(g) CO(g)+H2(g)。
CO(g)+H2(g)。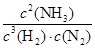 =
=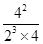 =0.5,这说明反应达到平衡状态,所以此时反应υ(N2)正=υ(N2)逆;A、正方应是体积减小的,则缩小体积增大压强,反应速率加快,平衡向正反应方向移动,氨气的含量增大,A正确;B、正方应是放热反应,升高温度反应速率加快,平衡向逆反应方向移动,氨气含量降低,B不正确;C、加催化剂加快反应速率,但平衡状态不变,氨气含量不变,C不正确;D、使氨气液化移走,平衡向正反应方向移动,但则反应速率降低,D不正确,答案选A。
=0.5,这说明反应达到平衡状态,所以此时反应υ(N2)正=υ(N2)逆;A、正方应是体积减小的,则缩小体积增大压强,反应速率加快,平衡向正反应方向移动,氨气的含量增大,A正确;B、正方应是放热反应,升高温度反应速率加快,平衡向逆反应方向移动,氨气含量降低,B不正确;C、加催化剂加快反应速率,但平衡状态不变,氨气含量不变,C不正确;D、使氨气液化移走,平衡向正反应方向移动,但则反应速率降低,D不正确,答案选A。 υ(C)正=2υ(C)逆,因此正逆反应速率不等,没有达到平衡状态,A不正确;B、A和B的转化率相等不能说明正逆反应速率相等,即反应不一定达到平衡状态,所以B不正确;C、正方应是体积减小的可逆反应,因此压强始终是减小,所以当容器内压强保持不变时可以说明反应达到平衡状态,C正确;D、密度是混合气的质量和容器容积的比值,在反应过程中容积始终是不变的,但气体的质量是减小的,所以当混合气体的密度保持不变时,可以说明反应达到平衡状态,D正确,答案选CD。
υ(C)正=2υ(C)逆,因此正逆反应速率不等,没有达到平衡状态,A不正确;B、A和B的转化率相等不能说明正逆反应速率相等,即反应不一定达到平衡状态,所以B不正确;C、正方应是体积减小的可逆反应,因此压强始终是减小,所以当容器内压强保持不变时可以说明反应达到平衡状态,C正确;D、密度是混合气的质量和容器容积的比值,在反应过程中容积始终是不变的,但气体的质量是减小的,所以当混合气体的密度保持不变时,可以说明反应达到平衡状态,D正确,答案选CD。

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.H2(g)的燃烧热为 -571.6 kJ·mol-1 |
| B.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多 |
C. H2SO4(aq)+ H2SO4(aq)+ Ba(OH)2(aq)= Ba(OH)2(aq)=  BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1 BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1 |
| D.3H2(g)+CO2(g)= CH3OH(l)+H2O(l) ΔH=+135.9 kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| B.1 mol S完全燃烧放热297.3 kJ,其热化学方程式:S+O2=SO2 ΔH=-297.3 kJ·mol-1 |
| C.1 mol H2SO4与1 mol Ba(OH)2反应生成1 mol BaSO4沉淀时放出的热量叫做中和热 |
| D.反应热的大小与反应物所具有的能量和生成物所具有的能量无关 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.C(s)+1/2O2(g)=CO(g) ΔH=-110.5kJ·mol-1 (燃烧热) |
| B.2H2O(g)=2H2(g)+O2(g) ΔH=+483.6 kJ·mol-1(反应热) |
| C.C2H5OH+3O2=2CO2+3H2O ΔH=-1368.8 kJ·mol-1(反应热) |
| D.2NaOH(aq)+H2SO4(aq)=Na2SO4 (aq)+2H2O(l) ΔH=-114.6 kJ·mol-1(中和热) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.③④⑦⑧ | B.①③④⑦⑧ | C.①②⑤⑥⑨ | D.①④⑦⑨ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
B.由N2O 4(g)  2NO2(g)△H=" -56.9" kJ·mol-1,可知将1mol N2O4(g)置于密闭容器中充分反应后放出热量为56.9kJ 2NO2(g)△H=" -56.9" kJ·mol-1,可知将1mol N2O4(g)置于密闭容器中充分反应后放出热量为56.9kJ |
| C.由:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,可知:含1mol CH3COOH的溶液与含1mol NaOH的溶液混合,放出热量为57.3 kJ |
| D.已知101kPa时,2C(s)+O2(g)===2CO(g) ΔH=-221kJ/mol,则1 mol碳完全燃烧放出的热量大于110.5kJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
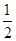 O2(g) ΔH=-226 kJ/mol
O2(g) ΔH=-226 kJ/mol| A.CO的燃烧热为283 kJ/mol |
B.下图可表示由CO生成CO2的反应过程和能量关系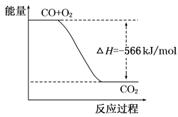 |
| C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-452 kJ/mol |
| D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为2×6.02×1023 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com