
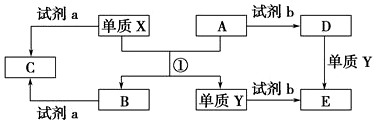
分析 X、Y是生活中用处广泛的两种金属单质,A、B是氧化物,A呈红棕色,则A为Fe2O3,反应①为铝热反应,所以X为Al,Y为Fe,B为Al2O3,试剂a为NaOH或HCl,则C为偏铝酸钠,试剂b为硫酸,则D为硫酸铁,E为硫酸亚铁,然后利用物质的性质及化学用语来解答;
解答 解:X、Y是生活中用处广泛的两种金属单质,A、B是氧化物,A呈红棕色,则A为Fe2O3,反应①为铝热反应,所以X为Al,Y为Fe,B为Al2O3,试剂a为NaOH或HCl,则C为偏铝酸钠,试剂b为硫酸,则D为硫酸铁,E为硫酸亚铁,
(1)反应①的化学方程式为Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,故答案为:Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3;
(2)根据上面的分析可知,试剂a为NaOH或HCl,
故答案为:NaOH或HCl;
(3)工业上用E、H2SO4和NaNO2为原料制取高效净水剂Y(OH)SO4,还原产物为N0,则该反应为2FeSO4+H2SO4+2NaNO2=2Fe(OH)SO4+Na2SO4+2NO↑,
故答案为:2FeSO4+H2SO4+2NaNO2=2Fe(OH)SO4+Na2SO4+2NO↑.
点评 本题考查无机物的推断,涉及Fe、Al元素单质化合物的性质,注意对铝热反应的掌握,在推断中经常涉及,难度中等.


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 羟基和氢氧根离子有相同的化学式和结构式 | |
| B. | 乙醇的官能团是羟基 | |
| C. | NaOH中含有羟基 | |
| D. | 乙醇与钠反应中,羟基被取代 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 序号 | ① | ② | ③ | ④ | ③ | ⑥ |
| 仪器及装置图 |  |  |  |  |  |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ | |
| B. | 稀硫酸与Ba(OH)2溶液混合:SO42-+Ba2+═BaSO4↓ | |
| C. | 稀硝酸滴在大理石上:CaCO3+2H+═Ca2++H2CO3 | |
| D. | 氧化铁与稀盐酸混合:Fe2O3+6H+═2Fe3++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶解粗盐时,应尽量让溶液稀些,防止食盐不完全溶解 | |
| B. | 滤去不溶性杂质后,将滤液移至坩埚内加热浓缩 | |
| C. | 将制得的晶体转移到新制过滤器中用大量水进行洗涤 | |
| D. | 当蒸发到剩余少量液体时,停止加热,利用余热将液体蒸干 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com