
【题目】下列有关有机物的构型判断错误的是( )
A. 甲烷是正四面体结构,烷烃的碳原子呈直线形
B. 乙烯是平面结构,1-丙烯三个碳原子共面
C. 苯分子中碳原子采用sp2杂化,得到平面正六边形结构
D. COCl2为平面结构分子
科目:高中化学 来源: 题型:
【题目】有关下列四个常用电化学装置的叙述正确的是( )
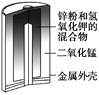
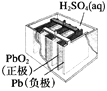
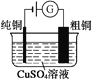
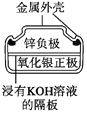
图1 碱性锌锰电池 图2 铅—硫酸蓄电池 图3 电解精炼铜 图4 银锌纽扣电池
A. 图1所示电池中,MnO2的作用是催化剂
B. 图2所示电池放电过程中,硫酸浓度不断增大
C. 图3所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D. 图4所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计计如下图所示装罝(部分夹持装置己略去)进行实验探究:
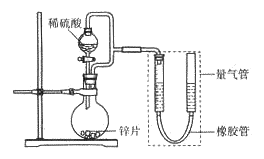
(1)用上述装置探究影响化学反应速率的因素。以生成9.0 mL气体为计时终点,结果为t1>t2。
序号 | V(H2SO4)/mL | C(H2SO4)/mol·L-1 | t/s |
I | 40 | 1 | t1 |
II | 40 | 4 | t2 |
①比较实验I和Ⅱ可以得出的实验结论是_______________。
②若将锌片换成含杂质的粗锌片,其他条件使其与上述一致,所测得的反应速率均大于上述实验对应的数据。粗锌片中所含杂质可能是_________(填序号)。
A.二氧化硅 B.银 C.铜 D.石墨
(2)用上述装置验证生铁在潮湿空气中会发生吸氧腐蚀。
①圆底烧瓶中的试剂可选用________(填序号)。
A.稀HCl B .NaCl溶液 C.乙醇 D.NaOH溶液
②能证明生铁在潮湿空气中会发生吸氧腐蚀的现象是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醚是一种淸洁燃料,以![]() =2的比例将混合气体通入1L的反应器中,一定条件下发生反应:2CO(g)+4H2(g)
=2的比例将混合气体通入1L的反应器中,一定条件下发生反应:2CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g) △H,其CO的平衡转化率随温度、压强变化关系如图所示,下列说法正确的是
CH3OCH3(g)+H2O(g) △H,其CO的平衡转化率随温度、压强变化关系如图所示,下列说法正确的是
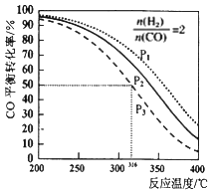
A. 上述反应△H<0
B. 图中P1<P2<P3
C. 若在P3和316℃时,测得容器中n(H2)=n(CH3OCH3),此时v(正)<v(逆)
D. 若在P3和316℃时,起始时![]() =3,则达到平衡时,CO转化率小于50%
=3,则达到平衡时,CO转化率小于50%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。下列有关说法正确的是
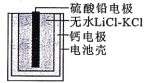
A. Ca为正极 B. 放电过程中,Li+向负极移动
C. 每转移0.2mol电子,理论上生成20.7gPb D. 电池工作一段时间后,正极质量增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容密闭容器中,发生反应:2NO2(g)![]() N2O4(g)。下列说法正确的是
N2O4(g)。下列说法正确的是
A. 混合气体平均相对分子质量不变时,反应达到平衡状态
B. 达到平衡后,两种物质的浓度之比为2:1
C. 升高温度,平衡状态不改变
D. 若平衡后压强是开始的0.8倍,则转化率为20%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种短周期元素在元素周期表中的位置关系如图:
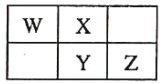
I.若Y元素原子的最外层电子数是电子层数的2倍。
(1)Z在周期表中的位置是___。
(2)写出铜和W的最高价氧化物的水化物的稀溶液反应的离子方程式:__________。
(3)Z最高价氧化物的水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有28mol电子发生转移时,共产生9mol气体,写出该反应的化学方程式:____________。
II.若X和Y的核外电子数之和为22。
(4)X的气态氢化物的电子式为______,将该氢化物通入硝酸溶液中,恰好反应时所得溶液中离子浓度大小的顺序为____________。
(5)W的单质与Z的最高价氧化物的水化物的浓溶液反应,当电子转移0.4mol时,产生气体的体积是_________(标准状况)。
(6)下列能比较Z元素与氯元素非金属性强弱的是_________。
A.氯气通入硫化钠溶液中,溶液变浑浊
B.盐酸是强酸,氢硫酸是弱酸
C.氯化氢比硫化氢稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将CH3CHO(易溶于水,沸点为20.8 ℃)和CH3COOH(易溶于水,沸点为117.9 ℃)分离的最合适方法是
A. 蒸馏
B. 加入Na2CO3溶液后,通过萃取的方法分离
C. 加入烧碱溶液之后蒸馏出乙醛,再加入浓硫酸,蒸馏出乙酸
D. 和Na反应后进行分离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,1mol 任何气体体积为22.4L.那么在标准状况下,700L NH3 的物质的量为________mol,全部溶解在1L水中,所得溶液的质量分数为________,如果该氨水的密度为0.85gcm﹣3 , 则氨水的体积为 ________L,物质的量浓度为________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com