
【题目】实验室用下列方法测定某水样中O2的含量。
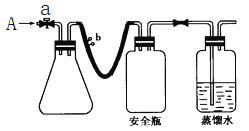
(1)实验原理
①用如图所示装置,使溶解在水中的O2在碱性条件下将Mn2+氧化成MnO(OH)2,反应的离子方程式为_____________________________。
②在酸性条件下,再用I-将生成的MnO(OH)2,还原为Mn2+,反应的离子方程式为_____________________________。然后用Na2S2O3标准溶液滴定生成的I2,反应方程式为I2+2 Na2S2O3=2Na1+Na2S4O6。
(2)实验步骤
①打开止水夹a和b,从A处向装置内鼓入过量N2,此操作的目的是___________________________;
②用注射器抽取某水样20. 00mL从A处注入锥形瓶;
③再分别从A处注入含m mol NaOH溶液及过量的MnSO4溶液;
④完成上述操作后,关闭a、b,将锥形瓶中溶液充分振荡;
⑤打开止水夹a、b,分别从A处注入足量NaI溶液及含n mol H2SO4的硫酸;
⑥重复④的操作;
⑦取下锥形瓶,向其中加入23滴_______作指示剂;
⑧用0.005 mol L -1 Na2S2O3溶液滴定至终点。滴定终点的现象是___________________________。
(3)数据分析
①若滴定过程中消耗的Na2S2O3标准溶液体积为3.90 mL,则此水样中氧(O2)的含量为________ mg L-1。
②若未用Na2S2O3标准溶液润洗滴定管,则测得水样中O2的含量将_________ (填“偏大”“偏小”或“不变”)。
【答案】 2 Mn2++O2+4OH-= MnO(OH)2+I2+3H2O MnO(OH)2+2I-+4H+=Mn2++I2+3H2O 排出装罝内的空气,避免空气中的O2的干扰 淀粉溶液 滴最后一滴标准液,溶液恰好由蓝色变为无色,且半分钟内不恢复原色 7.8 偏大
【解析】(1)①溶解在水中的O2在碱性条件下将Mn2+氧化成MnO(OH)2,锰元素化合价升高2价,氧气化合价降低了4价,根据化合价升高降低相等配平反应的离子方程式为:2Mn2++O2+4OH-=2MnO(OH)2;②在酸性条件下,再用I-将生成的MnO(OH)2,还原为Mn2+,而本身被氧化为碘单质,反应的离子方程式为:MnO(OH)2+2I-+4H+=Mn2++I2+3H2O;(2)①由于测定的是水样中氧气含量,必须将装置中的空气赶走,避免干扰测定结果,故答案为:赶走装置内空气,避免空气中的O2的干扰;⑦由于反应中有碘单质参与,利用碘遇到淀粉显示蓝色的特性,可以选用淀粉做指示剂;⑧用0.005 mol L -1 Na2S2O3溶液滴定至终点,碘消耗完,蓝色褪去。滴定终点的现象是:滴最后一滴标准液,溶液恰好由蓝色变为无色,且半分钟内不恢复原色;(3)①发生的反应有:2Mn2++O2+4OH-=2 MnO(OH)2、MnO(OH)2+2I-+4H+=Mn2++I2+3H2O、I2+2Na2S2O3=2NaI+Na2S4O=,
氧气反应的关系式为:O2~2MnO(OH)2~2I2~4Na2S2O3,
1000mL水样中含有的氧气的物质的量是:n(O2)=![]() n(Na2S2O3)×
n(Na2S2O3)×![]() =0.25×0.005molL-1×0.0039L×50=2.4375×10-4mol,
=0.25×0.005molL-1×0.0039L×50=2.4375×10-4mol,
氧气的质量为:2.4375×10-4mol×32g/mol=7.8mg,
此水样中氧(O2)的含量为7.8mgL-1;
②若未用Na2S2O3 标准溶液润洗滴定管,会导致标准液的浓度减小,消耗的标准液的体积增大,测定结果偏大。


科目:高中化学 来源: 题型:
【题目】(1)写出下图中序号①~④仪器的名称:
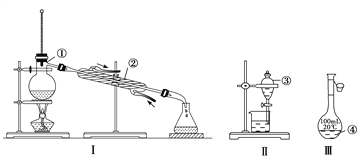
①___________;②___________; ③___________; ④___________。
(2)仪器①~④中,使用时必须检查是否漏水的有__________(填仪器序号)。
(3)右图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制480 mL 1 mol·L-l的稀硫酸。

可供选用的仪器有: ①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平。
请回答下列问题:
①配制稀硫酸时,还缺少的仪器有__________、__________(写仪器名称)。
②经计算,配制480 mL l mol·L-l的稀硫酸需要用量筒量取上述浓硫酸的体积为________mL。将量取好的浓硫酸缓慢注入到盛水的烧杯后,发现量筒里还残留有浓硫酸,如果用蒸馏水洗涤后一并将洗涤液注入烧杯,将使结果浓度______(填“偏高”“偏低”或“无影响”)。
③在转入容量瓶前烧杯中液体应_______,否则会使结果浓度____(填“偏高”“偏低”或“无影响”)。
④定容时必须使溶液的凹液面与刻度线相平,若俯视会使浓度______。(填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示的是钢铁在海水中的锈蚀过程,以下有关说法正确的是( )

A. 该金属腐蚀过程为析氢腐蚀
B. 正极为C,发生的反应为氧化反应
C. 在酸性条件下发生的是吸氧腐蚀
D. 正极反应为O2+2H2O+4e-===4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 化学实验的微型化可有效地减少污染,实现化学实验绿色化的要求。
某同学按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1 mol·L-1的KBr溶液、KI(含淀粉)溶液、NaOH(含酚酞)溶液、FeCl2(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如图所示),在圆心e处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,再立即将表面皿盖好。
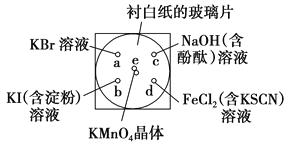
(1)e处反应的离子方程式为____________________________。
(2)b处的实验现象为_________________________________________。
(3)c处反应的化学方程式为____________________________________________。
标准状况下,当有0.224 L Cl2被NaOH溶液吸收后,转移电子的物质的量为________mol。
(4)通过该实验能否比较Cl2、FeCl3、KMnO4三种物质氧化性的强弱?________(填“能”或“不能”),若能,其氧化性由强到弱的顺序是________________。
II. 据报道,有一种细菌在有氧气存在的酸性溶液中,可将黄铜矿CuFeS2氧化成硫酸盐:4CuFeS2+2H2SO4+17O2===4CuSO4+2Fe2(SO4)3+2H2O。利用反应后的溶液,按如下流程可制备胆矾(CuSO4·5H2O):
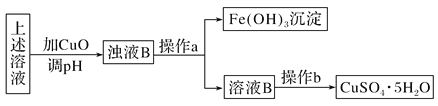
①检验溶液B中Fe3+是否被除尽的实验方法
_________________________________________________________________。
②在实验室中,设计两个原理不同的方案,从溶液B中提炼金属铜(要求:一种方案只用一个反应来完成)。写出两种方案中涉及的化学方程式:
方案一:_________________________________________________________;
方案二:_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】检验SO2气体中是否混有CO2气体,可采用的方法是( )
A. 通过品红溶液
B. 通过澄清石灰水
C. 先通过氢氧化钠溶液,再通过澄清石灰水
D. 先通过酸性高锰酸钾溶液,再通过澄清石灰水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用氯酸钾和浓盐酸反应来制取氯气,反应方程式如下:KClO3 + 6HCl(浓)== KCl + 3Cl2↑+ 3H2O
(1)该反应中发生还原反应的物质是__________。氧化产物是___________。
(2)当有0.2mol电子发生转移时,生成的氯气的体积为________L(标准状况)。被氧化的HCl的物质的量为______mol。
(3)将生成的氯气通入到石灰乳中,当两者恰好反应时,可制得漂白粉_________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收,设计了如图的装置。试回答下列问题:

(1)电源中电极a的名称是__________。(正极、负极)
(2)氯气被吸收时所发生反应的化学方程式为_______________。
(3)检验Cl2是否吸收完全,可采用的方法是______________。
(4)研究表明,当NaCl刚好电解完时,溶液中只有一种溶质,则该溶质最有可能是________________。由此可以用一个化学方程表示该容器中所发生的化学反应,该化学方程式为_______________。
(5)NaCl中往往含有CaCl2、MgSO4杂质,为了除去上述杂质,可选用A:BaCl2、B:Na2CO3、C:NaOH、D:HCl。
使用试剂正确的顺序为(________________________)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素x、y、z、m、n在元素周期表中的位置如图所示,则下列说法中错误的是
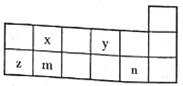
A. 最高价氧化物的水化物的酸性由弱到强的顺序是m、x、n
B. y、n分别与金属钠形成的化合物中均只含有离子键
C. y、z、n分别形成的简单离子半径的大小为n>y>z
D. x、z、m、n的最高价氧化物对应水化物均能与强碱反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com