
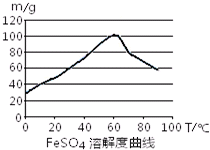
 铁盐、亚铁盐在工农业生产、生活、污水处理等方面有着极其广泛的应用.用铁屑与硫酸反应制备FeSO4
铁盐、亚铁盐在工农业生产、生活、污水处理等方面有着极其广泛的应用.用铁屑与硫酸反应制备FeSO4| n(Fe) |
| n(H2SO4) |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
 新华网2005年4月2日讯:美国研究人员在网络版《科学》杂志上发表论文说,他们开发出了一种新的固体氧化物燃料电池,在用碳氢化合物--异辛烷做燃料时,能源转换效率有望达到50%.采用异辛烷(iso-C8H18)的新型固体氧化物燃料电池,相当于把氧的提纯工厂“压缩”在一个小型装置中,而且异辛烷属于直链烃类,与汽油非常类似,不需要新建基础设施,因此这种燃料电池的前景非常可观.已知该电池的原理结构如图所示,中间阴影部分为固体氧化物陶瓷,可传递氧离子,下列有关说法错误的是( )
新华网2005年4月2日讯:美国研究人员在网络版《科学》杂志上发表论文说,他们开发出了一种新的固体氧化物燃料电池,在用碳氢化合物--异辛烷做燃料时,能源转换效率有望达到50%.采用异辛烷(iso-C8H18)的新型固体氧化物燃料电池,相当于把氧的提纯工厂“压缩”在一个小型装置中,而且异辛烷属于直链烃类,与汽油非常类似,不需要新建基础设施,因此这种燃料电池的前景非常可观.已知该电池的原理结构如图所示,中间阴影部分为固体氧化物陶瓷,可传递氧离子,下列有关说法错误的是( )| A、异辛烷和氧气不需要储存在电池内,可减小电池的体积 |
| B、氢燃料电池的优点是实现零排放,缺点是氢难以制得,同时氢的提纯和储存也较为困难 |
| C、原电池负极的电极反应式为2C8H18+50O2--100e-═16CO2+18H2O |
| D、通异辛烷的电极为电池的正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | ② | ③ | ④ | |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| pH | 11 | 11 | 3 | 3 |
| A、V1L④与V2L②溶液混合后,若混合后溶液pH=4,则V1:V2=9:11 |
| B、将①、④两种溶液等体积混合,所得溶液中:c (NH4+)>c(Cl-)>c(OH-)>c(H+) |
| C、分别加水稀释10倍、四种溶液的pH:①>②>③>④ |
| D、在①、②中分别加入适量的氯化铵晶体后,①的pH减小,②的pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol OH-的质量为17 g?mol-1 | ||
| B、二氧化碳的摩尔质量为44 g | ||
| C、铁原子的摩尔质量等于它的相对原子质量 | ||
D、一个钠原子的质量等于
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com