���
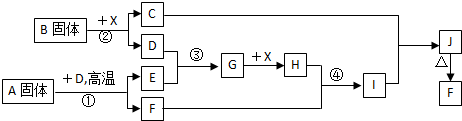
�⣺�������п�ͼ��ϵ��գ���֪��Ӧ�١������ҹ���ҵ�����е���Ҫ��Ӧ��X������Ϊ��ɫ��ζ��Һ���ƶ�Ϊˮ��C��ɫ��Ӧ����ʻ�ɫ˵������Ԫ�أ�JΪ���ɫ����Ϊ����������FΪFe
2O
3��D��E������Ϊ���壬��E��ʹƷ����Һ��ɫ˵��EΪSO
2��GΪSO
3��HΪH
2SO
4��IΪ��������˼· 1��3������Ӧ����D����1�Ǹ��������·�Ӧ�ģ���������DΪ������������Ӧ��������BΪ�������ƣ�CΪ�������ƣ�DΪ������A��D�ڸ����·�Ӧ���ɶ�������ͺ��������Ļ������ҵ�ϳ��õ������������е���Ҫ��Ӧ������Ĺ�ҵ����������Ĺ�ҵ����������Ĺ�ҵ����ԭ�϶�Ϊ������ͻ��������������ǻ���������AΪFeS
2��
��AΪFeS
2����BΪNa
2O
2��CΪNaOH��xΪH
2O����DΪ������EΪSO
2��FΪFe
2O
3��GΪSO
3��HΪ���ᣬIΪ��������JΪ����������
��1�����ݷ����жϽ����AΪ��FeS
2��FΪ Fe
2O
3��
�ʴ�Ϊ��FeS
2��Fe
2O
3��
��2����Ӧ���Ƕ�������������ķ�Ӧ����Ӧ����ʽΪ2SO
2+O
2 2 SO
3��
�ʴ�Ϊ��2SO
2+O
2 2 SO
3��
��3����Ӧ���ǹ���������ˮ��Ӧ����Ӧ�����ӷ���ʽΪ��2Na
2O
2+2H
2O=4Na
++4OH
-+O
2����
�ʴ�Ϊ��2Na
2O
2+2H
2O=4Na
++4OH
-+O
2����
��4����Ӧ�������������������ᷴӦ����Ӧ�����ӷ���ʽΪ��Fe
2O
3+6H
+=2Fe
3++3H
2O��
�ʴ�Ϊ��Fe
2O
3+6H
+=2Fe
3++3H
2O��
��5����֪ÿ����16g EΪSO
2�����ʵ���Ϊ0.25mol���ų�106.5kJ���������ݻ�ѧ����ʽ4FeS
2��s��+11O
2��g��=2Fe
2O
3��s��+8SO
2��g��������8molSO
2��������
=3408KJ����Ӧ���Ƕ���������������Ӧ���������������Ͷ�������Ӧ���Ȼ�ѧ����ʽΪ��4FeS
2��s��+11O
2��g��=2Fe
2O
3��s��+8SO
2��g������H=-3408 kJ/mol��FeS
2��s��+
O
2��g���T
Fe
2O
3��s��+2SO
2��g����H=-852 kJ/mol��
�ʴ�Ϊ��FeS
2��s��+
O
2��g���T
Fe
2O
3��s��+2SO
2��g����H=-852 kJ/mol��