
分析 氢硫酸既属于二元酸,又属于无氧酸;
盐酸既属于一元酸,又属于无氧酸;
硫酸既属于二元酸,又属于含氧酸;
碳酸既属于二元酸,又属于含氧酸.
HCl为一元酸、无氧酸,硫酸和碳酸都属于二元酸和含氧酸,其中盐酸和硫酸为强酸,碳酸为弱酸,并且硫酸沸点高,难挥发,以此分类.
解答 解:根据交叉分类法,请用斜线将下面框图的酸与酸的分类连接起来: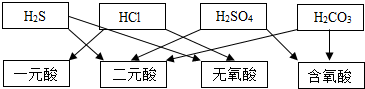
依据物质是否完全电离分为强酸HCl、H2SO4、弱酸为H2S、H2CO3,
依据酸的沸点高低可以分为高沸点酸硫酸,低沸点酸为HCl、H2S、H2CO3,
故答案为:
酸性强弱(或沸点高低),强酸、弱酸(或难挥发性酸、挥发性酸).
点评 本题考查溶液的物质的量浓度的计算以及物质的分类,题目难度不大,注意物质的分类标准和物质的性质.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
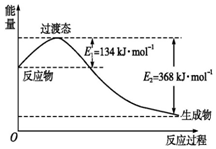 写出下列反应的热化学方程式
写出下列反应的热化学方程式查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.0 mol/L | B. | 0.50 mol/L | C. | 1.0 mol/L | D. | 0.10 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液 | B. | 悬浊液 | C. | 乳浊液 | D. | 胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应条件是加热的反应都是吸热反应 | |
| B. | 化学反应除了生成新的物质外,通常放出大量热 | |
| C. | 物质燃烧一定是放热反应 | |
| D. | 放热的化学反应不需要加热就能发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 化学反应中的能量变化都表现为热量变化 | |
| C. | 可逆反应达到化学平衡时,正、逆反应速率都为0 | |
| D. | 反应物和生成物所具有的总能量决定了反应是放热还是吸热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠溶液和稀盐酸反应:H++OH-═H2O | |
| B. | 大理石与盐酸反应制取二氧化碳:CO32-+2H+═H2O+CO2↑ | |
| C. | 铁粉投入盐酸溶液中:2Fe+6H+═Fe3++3H2↑ | |
| D. | 用小苏打治疗胃酸过多:CO32-+2H+═CO2↑+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com