
| 操作步骤 | 实验现象 | 解释原因 |
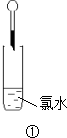 | 滴加硝酸银溶液,现象有:产生白色沉淀 | 原因有:氯气与水反应后,电离出Cl-,Cl-与Ag+生成AgCl白色沉淀 |
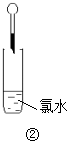 | 滴加紫色石蕊试液,现象有:先变红,后褪色 | 原因有:氯气与水反应后,溶液显酸性使紫色石蕊试液变红,产生的HClO又使红色的石蕊试液发生漂白 |
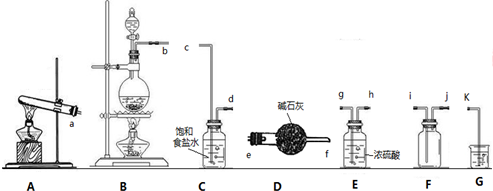
分析 (1)①实验室用二氧化锰和浓盐酸加热方法制取氯气,制备的氯气中含有氯化氢和水蒸气,依次通过盛有饱和食盐水、浓硫酸洗气瓶除去杂质,氯气密度大于空气密度,用向上拍空气法收集,尾气用氢氧化钠溶液吸收,据此排序;
②分析反应中元素化合价变化,依据得失电子守恒、原子个数守恒配平方程式;
③氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水;
(2)氯气溶于水,部分氯气与水反应生成氯化氢和次氯酸,氯化氢电离生成氢离子、氯离子,次氯酸部分电离生成氢离子和次氯酸根离子,次氯酸具有漂白性,据此解答.
解答 解:(1)①实验室用二氧化锰和浓盐酸加热方法制取氯气,制备的氯气中含有氯化氢和水蒸气,依次通过盛有饱和食盐水、浓硫酸洗气瓶除去杂质,氯气密度大于空气密度,用向上拍空气法收集,尾气用氢氧化钠溶液吸收,所以正确的连接顺序为:b→c→d→g→h→i→j→k;
故答案为:b、g、h;
②反应中锰元素化合价从+7价降为+2价,氯元素化合价从-1价升高为0价,依据氧化还原反应得失电子守恒、原子个数守恒,反应方程式:2KMnO4+16HCl(浓)=2MnCl2+5Cl2↑+2KCl+8 H2O;
故答案为:2 16 2 5 2 8 H2O;
③氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水,离子方程式:Cl2+2OH-=Cl-+ClO-+H2O;
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(2)氯气溶于水,部分氯气与水反应生成氯化氢和次氯酸,氯化氢电离生成氢离子、氯离子,次氯酸部分电离生成氢离子和次氯酸根离子,
氯水中滴加硝酸银溶液,则氯离子与银离子反应生成白色氯化银沉淀;
氯气溶于水,部分氯气与水反应生成氯化氢和次氯酸,氯化氢电离生成氢离子、氯离子,次氯酸部分电离生成氢离子和次氯酸根离子,次氯酸具有漂白性,滴加紫色石蕊试液后,因为溶液中含有氢离子,显酸性,所以紫色石蕊变红,又因为溶液中含有次氯酸具有漂白性,所以最终红色褪色;
故答案为:
| 操作步骤 | 实验现象 | 解释原因 |
 | 滴加 硝酸银溶液,现象有:产生白色沉淀 | 原因有:氯气与水反应后,电离出Cl-,Cl-与Ag+生成AgCl白色沉淀 |
 | 滴加 紫色石蕊试液,现象有:先变红,后褪色 | 原因有:氯气与水反应后,溶液显酸性使紫色石蕊试液变红,产生的HClO又使红色的石蕊试液发生漂白 |
点评 本题考查了氯气的实验室制备和氯水性质检验,明确氯气制备原理和氯水成分是解题关键,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| A. | 聚四氟乙烯有固定的熔点 | |
| B. | 合成ETFE及合成聚全氟乙丙烯的反应均为加聚反应 | |
| C. | 聚全氟乙丙烯分子的结构简式可能为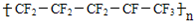 | |
| D. | ETFE分子中可能存在“-CH2-CH2-CF2-CF2-”的连接方式 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 现有下列四种物质,①H2②Cl2③SO2④H2SO4请回答相关问题:
现有下列四种物质,①H2②Cl2③SO2④H2SO4请回答相关问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 湿法炼铜和火法炼铜的反应中,铜元素都发生还原反应 | |
| B. | 加强热,使CuO在高温条件下分解制备单质Cu | |
| C. | 黑色金属材料包括铁、铬、锰及其化合物 | |
| D. | 生铁与钢的区别在于生铁含碳杂质,而钢不含 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.49g | B. | 3.60g | C. | 3.81g | D. | 3.92g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v正(N2)=v正(H2) | B. | v正(N2)=v逆(NH3) | ||
| C. | 2 v正(H2)=3 v逆(NH3) | D. | v正(N2)=v逆(H2) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验①生成的气体不能使湿润的KI-淀粉试纸变蓝 | |
| B. | 实验②证明Fe2+既有氧化性又有还原性 | |
| C. | 上述实验证明氧化性:MnO4->CI2>Fe3+>I2 | |
| D. | 上述实验中,共有两个氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-丁烯与HBr发生加成反应 | |
| B. | 3-氯戊烷与NaOH乙醇溶液共热发生消去反应 | |
| C. | 甲苯在一定条件下发生溴代反应生成一溴代甲苯的反应 | |
| D. | 邻羟基苯甲酸与NaHCO3溶液反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com