

| ||
| ||


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 除去悬浮 |
| 杂质 |
| 浓缩 |
| 氧化剂 |
| 氧化 |
| 热空气 |
| Na2CO3溶液 |
| 吸收 |
| H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
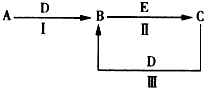
查看答案和解析>>
科目:高中化学 来源: 题型:
 的名称为4-苯基-2-丁醇.下列关于有机物的说法中,不正确的是( )
的名称为4-苯基-2-丁醇.下列关于有机物的说法中,不正确的是( )A、 的名称为3-苯基-2-丙醇 的名称为3-苯基-2-丙醇 |
| B、4-苯基-2-丁醇与苯甲醇互为同系物 |
| C、4-苯基-2-丁醇分子中的所有碳原子一定不共平面 |
| D、4-苯基-2-丁醇的核磁共振氢谱共有8个峰 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、滤出的不溶物一定是铜 |
| B、滤出的不溶物一定含铜,但不一定含铁 |
| C、滤出的不溶物一定是铁 |
| D、滤液中一定含有Fe2+和Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、属于非极性分子 |
| B、沸点低于CO2 |
C、电子式为 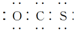 |
| D、三个原子位于同一直线上 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com