
����Ŀ��������Դ�����þ��й���ǰ����
��1�����辭����ѧ�仯���ܴӺ�ˮ�л�õ���������______��������ţ���
A��Cl2 B����ˮ C���ռ� D��ʳ��
��2����ͼ�ǴӺ�ˮ����ȡþ�ļ����̡�

�ٲ���A�� _______________________��
����ˮMgCl2������״̬�£�ͨ�������Mg��Cl2���÷�Ӧ�Ļ�ѧ����ʽΪ_____��
�ۺ�ˮ��þ�Ĺ��̣�ΪʲôҪ����ˮ�е��Ȼ�þת��Ϊ������þ����ת��Ϊ�Ȼ�þ��____��
��3���������и�����I����ʽ���ڵĵ�Ԫ�ء�ʵ������ȡI2��;��������ʾ��

�����պ������ҽ�ʱ���õ���Ҫ������������________��������ţ���
a������ b���Թ� c�������� d���ձ�
�����ữ����Һ�мӹ���������Һ��д���÷�Ӧ�����ӷ���ʽ________________��
����CCl4��ȡ��ʱ������CCl4������ѡ�õ��Լ�����________��������ĸ��ţ���
a���� b���Ҵ� c������
��Ϊ������CCl4��ȡ����ˮ��Һ���Ƿ��еⵥ�ʡ���д����ʵ���ʵ�鲽�衢�����ۣ�_______��
��4�����ú��ġ���ȼ����������ȼ�ϵ�ص��ܷ�ӦʽΪCH4+2O2+2KOH = K2CO3+3H2O�����ȼ�ϵ�صĸ����ĵ缫��ӦΪ__________________��
��5������ú���ۺ����ÿ����ĸ�����CO2�������״�ȼ�ϣ��䷴Ӧ�ķ���ʽΪ��
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)��ij��ѧʵ�齫6 mol CO2��8 mol H2����2 L���ܱ������У����H2�����ʵ�����ʱ��仯��ͼʵ����ʾ��a��b��c��d���������ݱ�ʾ���ꡣ
CH3OH(g)+H2O(g)��ij��ѧʵ�齫6 mol CO2��8 mol H2����2 L���ܱ������У����H2�����ʵ�����ʱ��仯��ͼʵ����ʾ��a��b��c��d���������ݱ�ʾ���ꡣ

��a������Ӧ����_________������ڡ����ڻ�С�ڡ���a���淴Ӧ���ʡ�
��ƽ��ʱCO2�����ʵ���Ũ����___________mol/L��
���ܹ�˵���÷�Ӧ�ﵽ��ѧƽ��״̬�ı�־��_______��˫ѡ����
A����λʱ��������1molCO2��ͬʱ����3mol H2
B�����������ܶȲ���ʱ��仯
C��CH3OH��H2��Ũ�Ȳ�����ʱ��仯
D��CH3OH��H2OŨ�����
���𰸡� BD ���� MgCl2�����ڣ�![]() Mg + Cl2�� ��ˮ���Ȼ�þ�ĺ����ܴ�þ����Ũ�Ⱥܵͣ��ù��̿���ʹþ���Ӹ�����Ũ�ȸߣ��ҳɱ��� a H2O2+2I- +2H+ = I2+2H2O a ȡ������Һ���Թ��У��μӵ�����Һ������Һ����ɫ����˵����Һ���еⵥ�� CH4+10OH--8e-= CO32��+7H2O ���� 2mol/L AC
Mg + Cl2�� ��ˮ���Ȼ�þ�ĺ����ܴ�þ����Ũ�Ⱥܵͣ��ù��̿���ʹþ���Ӹ�����Ũ�ȸߣ��ҳɱ��� a H2O2+2I- +2H+ = I2+2H2O a ȡ������Һ���Թ��У��μӵ�����Һ������Һ����ɫ����˵����Һ���еⵥ�� CH4+10OH--8e-= CO32��+7H2O ���� 2mol/L AC
����������1����ˮ�������Եõ���ˮ�����ҿ������Ȼ��ƣ���Ϊ�����仯��
��2����ʯ������뺣ˮ�У���Ӧ����Mg(OH)2 ��������Һ��ͨ�����˵ķ�����Mg(OH)2 �����˳���
������״̬�µ���Ȼ�þұ��þ����ⷴӦ����ʽMgCl2�����ڣ�![]() Mg + Cl2��
Mg + Cl2��
�ۺ�ˮ���Ȼ�þ�ĺ����ܴ�þ����Ũ�Ⱥܵͣ��ù��̿���ʹþ���Ӹ�����Ũ�ȸߣ��ҳɱ��ͣ����Ժ�ˮ��þ�Ĺ��̣�ΪʲôҪ����ˮ�е��Ȼ�þת��Ϊ������þ����ת��Ϊ�Ȼ�þ��
��3�������չ���ʱ���õ���Ҫ����������������
�ڼ��������Ӻ��������������Ϊ����������������ת��Ϊ���ʵ⣬���ӷ���ʽΪH2O2+2I- +2H+ = I2+2H2O��
����ȡ��ʱ���õ�����ȡԭ��������Ҫ����DZ���
��Ϊ������CCl4��ȡ����ˮ��Һ���Ƿ��еⵥ�ʡ������õ�����������ķ�Ӧ����ʵ�鷽����ȡ������Һ���Թ��У��μӵ�����Һ������Һ����ɫ����˵����Һ���еⵥ����
��4��CH4ʧȥ���ӣ�����������Ӧ���Ǹ�������缫��ӦʽΪ��CH4+10OH--8e-= CO32��+7H2O ��
��5���ٴ�ͼ�п�֪��a�㻹û�е��ﻯѧƽ��״̬����ʱ����Ӧ���ʴ����淴Ӧ���ʡ�
����ͼ�п�֪���ӵ�8min����n(H2)���ٸı䣬˵���Ѵﵽ��ѧƽ��״̬����ʱn(H2)=2 mol����H2������6 mol����CO2�����ʵ���������2 mol��ƽ��ʱΪ4mol����ƽ��ʱCO2�����ʵ���Ũ����c(CO2)=4mol/2L=2 mol/L��
��A����λʱ��������1molCO2��ͬʱ����3mol H2����ʾ�������淴Ӧ��Ҳ���㻯ѧ��������ϵ��˵���÷�Ӧ�ﵽƽ��״̬����A��ȷ��B���������������ʾ�Ϊ���壬������������䣬���������غ㣬��Ӧǰ���������䣬���Ҳ���䣬�ܶȲ��䣬����˵����Ӧ�ﵽƽ��״̬��B
����C��CH3OH��H2��Ũ�Ȳ�����ʱ��仯��˵���Ѵﵽƽ��״̬��C��ȷ��D��CH3OH��H2OŨ����ȣ�����˵���Ƿﻯѧƽ��״̬��D����


 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ԫ���������о�Ԫ�ؼ��仯��������ʾ�����Ҫ�����塣
I.���ֶ���������Ԫ�ص�����������Ӧ��ˮ���Ũ�Ⱦ�Ϊ0.01mol.L-1)��Һ��pH��ԭ�������Ĺ�ϵ��ͼ��ʾ��
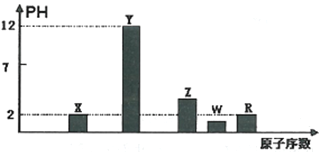
��1��Ԫ��R�����ڱ��е�λ����______________��Ԫ��Z��ԭ�ӽṹʾ��ͼ��__________��
��2��Ԫ��Y��W�γɵ�Y2W2�ͻ������к��л�ѧ��������Ϊ_____________��
II.������Ԫ��C��O��S���γɶ��ֻ������CO2��CS2��COS�ȡ�
��1��������˵��̼��������Ԫ�طǽ��������ǿ������____________������ţ�
A. S��H2�������Ϸ�Ӧ��C��H2���ϸ�����
B.����:H2SO3 >H2CO3
C.CS2��̼Ԫ��Ϊ+4�ۣ���Ԫ��Ϊ-2��
��2��Ǧ��Pb��������Sn�����ࣨGe����Ԫ��Cͬ���塣�������䵥���ڿ����У��������Ӧ����Ǧ���������һ������Ǧ�����������Ӧ�����������ᷴӦ���ɴ˿ɵó����½��ۣ�
�����ԭ������Ϊ__________________��
������+4����������ļ�����ǿ����˳��Ϊ_________________���ѧʽ����
��3���ʻ���COS������Ϊһ��Ѭ�������ܷ�ֹijЩ���桢�߳��Σ��������ӽṹ��CO2���ơ��õ���ʽ��ʾ�ʻ���COS�����γɹ��̣�________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������ܹ��ﵽʵ��Ŀ�ĵ���( )
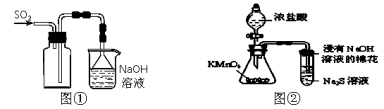
A��ʵ���Ҳ���ͼ����ʾװ���ռ�SO2
B������ͼ����ʾװ�ñȽ�KMnO4��Cl2��S��������ǿ��
C��ʵ�������Ȼ�̼�г����������壬�������ı��������ú��Һ���ɳ�ȥ���Ȼ�̼�е���
D����ȡ0.40 g NaOH��ֱ������100 mL����ƿ�м�ˮ���̶��ߣ�������0.10mol/L NaOH��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������ԭ��Ӧ���з�Ӧ��������ﹲ���֣� NO��FeSO4��Fe(NO3)3�� H2O�� HNO3�� Fe2(SO4)3������ HNO3Ϊ��Ӧ���÷�Ӧ�еĻ�ԭ��Ϊ( )
A�� NO B�� FeSO4 C��Fe(NO3)3 D��Fe2(SO4)3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����ӷ���ʽ��д��ȷ����
A���Ȼ�����Һ�м��������ˮ��Al3++4NH3H2O=AlO2-+4NH4++2H2O
B������ϡ���ᷴӦ��2Fe+6H+=2Fe3++3H2��
C��̼������ڴ��CaCO3+2H+=Ca2++CO2��+H2O
D���Ȼ�������Һ��ͨ��������2Fe2++Cl2=2Fe3++2Cl-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͬ���������и�������ȫȼ�պ�����H2O������
A. ����B. ��ϩC. ��ȲD. ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������Ϳ�����Ӧ��ʮ�ֹ㷺��
��1����CO2��NH3Ϊԭ�Ϻϳ����ص���Ҫ��Ӧ���£�
2NH3(g)+CO2(g)=NH2CO2NH4(s) ��H=��159kJ��mol��1
NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ��H=+72kJ��mol��1
H2O(l)=H2O(g) ��H=+44kJ��mol��1
��Ӧ2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l) ��H=______kJ��mol��1
��2��ij�¶��£����ݻ�Ϊ100 ml���ܱ�������ͨ��4molNH3��2molCO2������Ӧ2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g)������X��Ũ�ȱ仯��������ͼ��ʾ��
CO(NH2)2(s)+H2O(g)������X��Ũ�ȱ仯��������ͼ��ʾ��
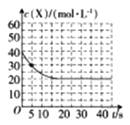
��ǰ5s�ڣ�v(H2O)=__________��
�ڸ������µ�ƽ�ⳣ��K=_______��
��3��T��ʱ���������ʵ�����NO��CO�������Ϊ2L���ܱ������У������¶Ⱥ�������䣬��Ӧ���̣�0����15min����NO�����ʵ�����ʱ��ı仯��ͼ��ʾ��
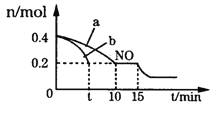
��ƽ��ʱ�������¶Ȳ��䣬���������г���CO��N2��0.8mol��ƽ�⽫____����������ҡ��������ƶ���
��ͼ��a��b�ֱ��ʾ��һ���¶��£�ʹ��������ͬ���������ͬ�Ĵ���ʱ���ﵽƽ�������n(NO)�ı仯���ߣ����б�ʾ����������ϴ��������______���a����b������
��15minʱ�����ı���練Ӧ����������n(NO)������ͼ��ʾ�ı仯����ı������������____��
��4����������Һ�к��д����İ������ʣ���NH3��ʾ�����Ȼ������������Һ������ͼ��ʾ�ĵ��أ��缫Ϊ���Բ��ϣ��н��е���ȥNH3��������ˮ���þ������̷���������һ�����������������ڶ�������������������������N2��
��д���ڶ�����Ӧ�Ļ�ѧ����ʽ_________��
������������Һ�а������ʵĺ���Ϊ1.7%���������ϵ��1t����ˮ����·��ת�Ƶĵ�����Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(CeO2)��һ����Ҫ��ϡ�����������Է�̼���(��Ҫ��CeFCO3)Ϊԭ���Ʊ� CeO2��һ�ֹ����������£�
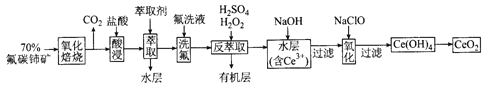
��֪����Ce4+����F-��ϳ�[CeFx](4-x)+��Ҳ����SO42-��ϳ�[CeSO4]2+��
����������ϵ��Ce4+�ܱ���ȡ��[(HA)2 ]��ȡ����Ce3+���ܡ�
�ش��������⣺
��1��������������ǰ�轫��ʯ�����ϸ��������Ŀ����_____________��
��2����������л������������ɫ���壬д��CeO2�����ᷴӦ�����ӷ���ʽ��____________��Ϊ�������������Ⱦ�������һ�ֽ��������_____________��
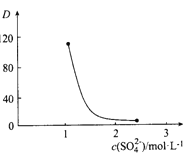
��3������ȡ��ʱ���ڷ�Ӧ��Ce4+ +n(HA)2![]() Ce��(H2n-4A2n)+4H+��ʵ��������ȡʱ�õ�����Ҫ������������Ϊ____________����ͼ��Dʱ����ȣ���ʾCe(��)�ֱ����л�������ˮ���д�����ʽ�����ʵ���Ũ��֮��(
Ce��(H2n-4A2n)+4H+��ʵ��������ȡʱ�õ�����Ҫ������������Ϊ____________����ͼ��Dʱ����ȣ���ʾCe(��)�ֱ����л�������ˮ���д�����ʽ�����ʵ���Ũ��֮��(![]() )�����������������䣬����ʼ��Һ�м��벻ͬ����Na2SO4�Ըı�ˮ���е�c(SO42-)��D����ʼ��Һ��c(SO42-)�仯��ԭ��__________��
)�����������������䣬����ʼ��Һ�м��벻ͬ����Na2SO4�Ըı�ˮ���е�c(SO42-)��D����ʼ��Һ��c(SO42-)�仯��ԭ��__________��
��4��������ȡ���У���ϡ�����H2O2��������CeO2ת��ΪCe3+��H2O2�ڸ÷�Ӧ����_________(��������������������������ԭ����)��ÿ��1molH2O2�μӷ�Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ__________��
��5��������������Ļ�ѧ����ʽΪ_____________��
��6��ȡ���������еõ���CeO2��Ʒ0.4500 g���������ܽ����0.1000mol/LFeSO4����Һ�ζ����յ�ʱ(������ԭΪCe3+���������ʾ�����Ӧ)������25.00 mL����Һ���ò�Ʒ��CeO2����������Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A��Һ̬�Ȼ��⡢�����Ȼ��ƾ������磬�����Ȼ��⡢�Ȼ��ƾ��Ƿǵ����
B��ͭ˿�ܵ��磬����ͭ˿�ǵ����
C��NH3��SO2��ˮ��Һ���ܵ��磬����NH3��SO2���ǵ����
D�����ǡ��ƾ���ˮ��Һ���ۻ�״̬�¾������磬���������Ƿǵ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com