
分析 依据浓硫酸的酸性,强氧化性、脱水性、吸水性结合现象解答,注意铜与浓硫酸反应过程中硫酸中部分硫元素化合价升高、部分化合价降低,据此判断解答.
解答 解:因浓硫酸具有吸水性,浓硫酸吸水稀释而放出大量的热,浓硫酸将蔗糖中的H和O以2:1的形式脱去,蔗糖变黑;浓硫酸具有强氧化性:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,产生有刺激性气味的气体,说明浓硫酸具有强氧化性 脱水性 吸水性;
浓硫酸露置空气中质量增加是因为浓硫酸具有吸水性,吸收空气中的水蒸气,说明浓硫酸具有吸水性;
铁制容器盛放浓硫酸,是因为浓硫酸具有强的氧化性,常温下使铁钝化形成致密氧化膜,阻止反应进行,体现浓硫酸强的氧化性;
热的浓硫酸和铜反应生成硫酸铜、二氧化硫和水,体现浓硫酸强的氧化性和酸性;
故答案为:①②③;③;①;①④.
点评 本题主要考查了浓硫酸的性质,明确浓硫酸的强氧化性、脱水性、吸水性三大特性及硫酸的酸性是解题关键,题目难度不大,注意脱水性与吸水性区别.


科目:高中化学 来源: 题型:解答题


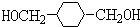 .
.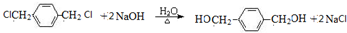 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
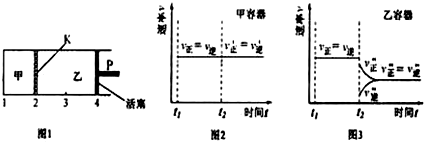
| A. | 保持温度和活塞位置不变,在甲中再加入1molA和2molB,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 | |
| B. | 保持活塞位置不变,升高温度,达到新的平衡后,甲中B的体积分数增大,乙中B的体积分数减小 | |
| C. | 保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 | |
| D. | 保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
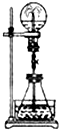 喷泉实验是一种常见的自然现象,其产生原因是存在压强差.在图中的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是( )
喷泉实验是一种常见的自然现象,其产生原因是存在压强差.在图中的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是( )| A. | Cu与稀盐酸 | B. | NH4HCO3与稀盐酸 | ||
| C. | CaCO3与稀硫酸 | D. | NaHCO3与NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A组 | B组 |
| Ⅰ.H2O分子间存在氢键,H2S则无 | ①H2O比H2S稳定 |
| Ⅱ.晶格能NaI比NaCl小 | ②NaCl比NaI熔点低 |
| Ⅲ.晶体类型不同 | ③N2分子比磷的单质稳定 |
| Ⅳ.元素第一电离能大小与原子外围电子排布有关,不一定像电负性随原子序数递增而增大 | ④同周期元素第一电离能大的,电负性不一定大 |
| A. | Ⅰ① | B. | Ⅱ② | C. | Ⅲ③ | D. | Ⅳ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com