
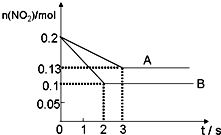
 在容积为VL的密闭容器中发生反应:2NO2(g)?2NO(g)+O2(g).反应过程中NO2的物质的量随时间变化的情况如图所示.曲线A和B表示的是该反应在不同条件下的反应状况,则该不同条件是( )
在容积为VL的密闭容器中发生反应:2NO2(g)?2NO(g)+O2(g).反应过程中NO2的物质的量随时间变化的情况如图所示.曲线A和B表示的是该反应在不同条件下的反应状况,则该不同条件是( )| A. | 起始浓度不同 | B. | 有、无催化剂 | C. | 温度不同 | D. | 压强不同 |
科目:高中化学 来源: 题型:解答题

 2OH-+H2↑+Cl2↑;.
2OH-+H2↑+Cl2↑;.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原电池的正极和电解池的阳极所发生的反应 | |
| B. | 原电池的阳极和电解池的负极所发生的反应 | |
| C. | 原电池的负极和电解池的阳极所发生的反应 | |
| D. | 原电池的负极和电解池的阴极所发生的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸钠晶体溶于水中 | |
| B. | NH4HCO3(s)分解生成NH3(g)、CO2(g)和H2O(g) | |
| C. | 水结成冰 | |
| D. | 干冰升华 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应是放热还是吸热,取决于生成物和反应物具有的总能量的相对大小 | |
| B. | 吸热反应在常温下不能发生 | |
| C. | 放热反应也可能需要加热才能发生 | |
| D. | 化学反应除了生成新物质外,还伴随着能量的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在如图中,甲烧杯中盛有100mL 0.50mol/L AgNO3溶液,乙烧杯中盛有100mL 0.25mol/L CuCl2溶液,A、B、C、D均为质量相同的石墨电极,如果电解一段时间后,发现A极比C极重1.9g.
在如图中,甲烧杯中盛有100mL 0.50mol/L AgNO3溶液,乙烧杯中盛有100mL 0.25mol/L CuCl2溶液,A、B、C、D均为质量相同的石墨电极,如果电解一段时间后,发现A极比C极重1.9g.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钡溶液与硫酸的反应 OH-+H+=H2O | |
| B. | 澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+=Ca2++2H2O | |
| C. | 铜片插入硝酸银溶液中 Cu+Ag+=Cu2++Ag | |
| D. | 碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | M层上有2对成对电子 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
| J | J的气态氢化物与J的最高价氧化物对应的水化物可反应生成一种盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用NaOH溶液吸收Cl2制备消毒液:Cl2+2OH-→Cl-+ClO-+H2O | |
| B. | 该消毒液与洁厕灵混用会引起中毒:2H++Cl-+ClO-→Cl2↑+H2O | |
| C. | 常温下,该消毒液的pH≈12是因为:ClO-+H2O?HClO+OH- | |
| D. | 该消毒液加少量白醋可增强消毒能力:CH3COOH+ClO-→HClO+CH3COO- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com