
���� ��1��ƫ�����£�C2H8N2����ȼ�ϣ������������������������ɵ����Ͷ�����̼���壬�Դ˿�д����ѧ����ʽ��
��2���÷�Ӧ���ṩ�ɴ����������������˵����Ӧ�ͷ�������Ϊ���ȷ�Ӧ��
��� �⣺��ƫ�����£�C2H8N2����ȼ�ϣ������������������������ɵ����Ͷ�����̼���壬�ʻ�ѧ����ʽΪ��C2H8N2+2N2O4$\frac{\underline{\;��ȼ\;}}{\;}$2CO2��+3N2��+4H2O��
�ʴ�Ϊ��C2H8N2+2N2O4$\frac{\underline{\;��ȼ\;}}{\;}$3N2+2CO2+4H2O��
�ڸ÷�Ӧ���ṩ�ɴ�����������������ʴ˷�ӦΪ���ȷ�Ӧ����Ӧ�����������������������������ʴ�Ϊ�����ȣ� ���ڣ�
���� ���⿼���˻�ѧ����ʽ����д�ͷ�Ӧ�����ȵ��жϣ�Ϊ��Ƶ���㣬���ؿ���ѧ���ķ��������ͷ�Ӧ�ȡ��ʱ�����⣬�ѶȲ���Ӧע����Ƿ�Ӧ������ȡ���ڷ�Ӧ��������������������Դ�С��ϼ����������ͳɼ��ų���������Դ�С��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
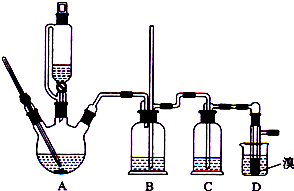
| �Ҵ� | 1��2-�������� | ���� | |
| ״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
| �ܶ�/g•cm-3 | 0.79 | 2.2 | 0.71 |
| �е�/�� | 78.5 | 132 | 34.6 |
| �۵�/�� | һl30 | 9 | -1l6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
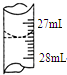 ���ⶨijNaOHmol•L-1��Һ�����ʵ���Ũ�ȣ�����0.100��HCl����Һ�����к͵ζ����ü�����ָʾ������
���ⶨijNaOHmol•L-1��Һ�����ʵ���Ũ�ȣ�����0.100��HCl����Һ�����к͵ζ����ü�����ָʾ������| ʵ����� | ����NaOH��Һ�����/mL | 0.1000mol•L-1HCl��Һ�����/mL | |
| �ζ�ǰ�̶� | �ζ���̶� | ||
| 1 | 25.00 | 0.00 | 26.29 |
| 2 | 25.00 | 1.00 | 31.00 |
| 3 | 25.00 | 1.00 | 27.31 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ѧ�� | H-H | C-O | C�TO | H-O | C-H |
| E/��kJ•mol-1�� | 436 | 343 | 1076 | 465 | 413 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com