
取pH值均等于2的盐酸和醋酸各120ml分别稀释2倍后,再分别加入0.03g锌粉,在相同条件下充分反应,有关叙述正确的是
A.醋酸与锌反应放出氢气多
B.盐酸和醋酸分别与锌反应放出的氢气一样多
C.醋酸与锌反应速率大
D.盐酸和醋分别与锌反应的速度一样大
科目:高中化学 来源: 题型:
化学在生产和日常生活中有着重要的应用。下列说法不正确的是( )
A.明矾水解形成的Al(OH)3胶体能吸附水中的悬浮物,可用于水的净化
B.在海轮的外壳镶上锌块,可减缓船体的腐蚀速率
C.用热的纯碱溶液洗碗去污效果好
D.电解熔融的AlCl3可制得金属铝
查看答案和解析>>
科目:高中化学 来源: 题型:
在pH=0的无色透明溶液中,因发生氧化还原反应而不能大量共存的离子组是 ( )
A.Na+、K+、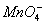 、
、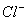 B.
B.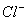 、
、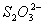 、K+、Na+
、K+、Na+
C.Na+、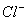 、
、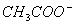 、K+ D.K+、
、K+ D.K+、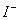 、Na+、
、Na+、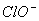
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下纯水中C(H+) = 2×12-7 mol/L,则此时溶液中的C(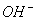 ) = ___________。
) = ___________。
若温度不变,滴入稀盐酸使C(H+) = 5×12-6 mol/L,则此时溶液中的C(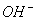 ) = ___________。
) = ___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列浓度关系正确的是
A. 氯水中:c(Cl2)=2[c(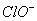 )+c(
)+c(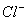 )+C(HClO)]
)+C(HClO)]
B. 氯水中:c(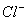 )>c(
)>c(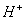 )>c(
)>c(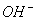 )>c(
)>c(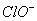 )
)
C. 等体积等浓度的氢氧化钠与醋酸混合:c(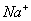 )=c(
)=c(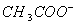 )
)
D. 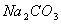 溶液中:c
溶液中:c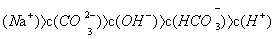
查看答案和解析>>
科目:高中化学 来源: 题型:
在甲烧杯中放入盐酸,乙烧杯中放入醋酸,两种溶液的体积和pH值都相等,向两烧杯中同时加入质量不等的锌粒,反应结束后得等量的氢气。下列说法正确的是:
A.甲烧杯中放入锌的质量比乙烧杯中放入锌的质量大;
B.甲烧杯中的酸过量;
C.两烧杯中参加反应的锌等量;
D.反应开始后乙烧杯中的c(H+)始终比甲烧杯中的c(H+)小。
查看答案和解析>>
科目:高中化学 来源: 题型:
欲使NaHCO3溶液中的c(H+)、c(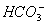 )、c(
)、c(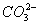 )都减少,其方法是 ( )
)都减少,其方法是 ( )
A.通入CO2气体 B.通入HCl气体
C.加入NaOH固体 D.加入Ca(OH)2固体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列措施对增大反应速率明显有效的是
A.在炭粉燃烧中加入KClO3
B.Zn与25%的稀硫酸反应制取H2时,改用98%的浓硫酸
C.在K2S04与BaCl2两溶液反应时,增大压强
D.Na与乙醇反应时增大乙醇的用量
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F、G是原子序数依次增大的七种元素,其中A、B、C、D、E为短周期元素,F、G为第四周期元素。已知:A是原子半径最小的元素,B、C、D是紧邻的三个族的元素,C的三价阴离子和E的二价阳离子具有相同的电子层结构,F元素的基态原子具有六个单电子,G的核电荷数比F多5。请回答下列问题(用相应的元素符号、化学式和化学术语填空)
(1)G在周期表中的位置是__________,F元素的原子基态价层电子排布式为__________。
(2)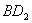 分子的电子式为__________,
分子的电子式为__________,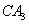 分子的空间立体构型为__________。
分子的空间立体构型为__________。
(3)A元素分别与B、D元素形成的两种微粒H、I都具有N2H4相似的结构,属于等电子数微粒,它们的化学式分别是H:__________、I:__________。
(4)向G的硫酸盐溶液中逐滴加入足量的氨水至得到的沉淀完全溶解,再向该溶液中加入一定量乙醇,析出一种深蓝色晶体。在该晶体中存在的化学键的种类有__________。
(5)0.3g H在足量氧气中燃烧,生成气态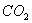 和液态
和液态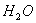 ,放出Q kJ热量,则表示H的燃烧热的热化学方程式为____________________。某燃料电池用H作燃料,KOH为电解液,该电池的负极电极反应式为:________________________________________。
,放出Q kJ热量,则表示H的燃烧热的热化学方程式为____________________。某燃料电池用H作燃料,KOH为电解液,该电池的负极电极反应式为:________________________________________。
(6)G的一种氧化物的晶胞结构如图所示(黑球代表G原子),该氧化物的化学式为____________________。
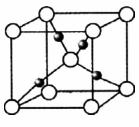
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com