
| A. | Al2O3、SO2、CO2、SO3 | B. | CO2、Cl2、CaO、SO3 | ||
| C. | Cl2、Al2O3、SO2、SO3 | D. | SiO2、CO2、CO、Cl2 |
分析 A.氧化铝与氢氧化钠反应生成偏铝酸钠,SO2、CO2、SO3与过量的氢氧化钠反应分别生成亚硫酸钠、碳酸钠、硫酸钠;
B.CaO与氢氧化钠不反应,氯气与氢氧化钠反应生成氯化钠、次氯酸钠,CO2、SO3与过量的氢氧化钠反应分别生成碳酸钠、硫酸钠;
C.氯气与氢氧化钠反应生成氯化钠、次氯酸钠,Al2O3、SO2、SO3与过量的氢氧化钠反应分别生成偏铝酸钠、亚硫酸钠、硫酸钠;
D.CO不与氢氧化钠反应,氯气与氢氧化钠反应生成氯化钠、次氯酸钠,SiO2、CO2与过量的氢氧化钠反应分别生成硅酸钠、碳酸钠.
解答 解:A、A12O3是两性氧化物与过量氢氧化钠反应生成的盐为偏铝酸钠;SO2与过量NaOH溶液反应生成的盐为亚硫酸钠;CO2与过量NaOH溶液反应生成的盐为碳酸钠;SO3与过量NaOH溶液反应生成的盐为硫酸钠,共有4种盐生成,故A不符合;
B、CO2与过量NaOH溶液反应生成的盐为碳酸钠;C12与过量NaOH溶液反应生成的盐为氯化钠和次氯酸钠;CaO与过量NaOH溶液不反应;SO3与过量NaOH溶液反应生成的盐为硫酸钠,共有4种盐生成,故B不符合;
C、C12与过量NaOH溶液反应生成的盐为氯化钠和次氯酸钠;A12O3与过量NaOH溶液反应生成的盐为偏铝酸钠;SO2与过量NaOH溶液反应生成的盐为亚硫酸钠;SO3与过量NaOH溶液反应生成的盐为硫酸钠,共有5种盐生成,故C符合;
D、SiO2与过量NaOH溶液反应生成的盐为硅酸钠;CO2与过量NaOH溶液反应生成的盐为碳酸钠;CO与过量NaOH溶液不反应;C12与过量NaOH溶液反应生成的盐为氯化钠和次氯酸钠,共有4种盐生成,故D不符合;
故选C.
点评 本题考查常见物质的性质,比较基础,掌握物质的性质是关键,解题时注意氢氧化钠过量.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | ②③④ | B. | ④ | C. | ① | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 实验装置 |  | 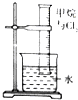 | 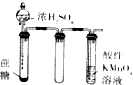 | 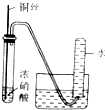 |
| 实验目的 | 提取苯中的Br2 | 探究甲烷的取代反应 | 检验浓硫酸的脱水性和强氧性 | 实验室制备并收集NO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4Br的电子式  | |
| B. | S2-的结构示意图  | |
| C. | 乙烯的分子式 CH2=CH2 | |
| D. | 原子核内有l7个中子的氯原子${\;}_{17}^{35}$Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该化学反应的过程是吸热的 | |
| B. | 该化学反应的过程是放热的 | |
| C. | 分子运动速率加快,使反应物分子的碰撞机会增多 | |
| D. | 反应物分子的能量增加,活化分子百分数增加,有效碰撞次数增多 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验方案 |
| A | 检验食盐中是否添加KIO3 | 取食盐试样,溶于KI溶液,加入淀粉溶液,观察溶液是否变蓝 |
| B | 验证硝酸是挥发性酸 | 用两根玻璃棒分别蘸取浓硝酸和浓氨水,然后靠近,观察是否有白烟产生 |
| C | 验证Br2氧化性强于Fe3+ | 取少许FeCl3晶体溶于稀盐酸,加入KSCN观察溶液是否变红,滴入溴水后再观察是否变红 |
| D | 验证氯酸钾中含有氯元素 | 取少量氯酸钾加入MnO2充分加热,残留物溶于水,取上层清液,滴入硝酸酸化的AgNO3溶液,观察是否有白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶质的质量分数为w=$\frac{a}{Vρ-a}$×100% | |
| B. | 上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w | |
| C. | 上述溶液中再加入相同质量的水后,所得溶液的物质的量浓度变为原来一半 | |
| D. | 溶质的物质的量浓度c=$\frac{1000a}{17V}$ mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com