
【题目】下列溶液中,氯离子浓度最大的是( )
A.1L 1mol/L NaCl溶液B.2L 1mol/L KCl溶液
C.3L 1mol/L AlCl3溶液D.1L 2mol/L NaCl溶液
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知在25℃、1.013×105Pa下,1mol氢气完全燃烧生成液态水放出285kJ的热量,请回答下列问题:
(1)生成物能量总和__________(填"大于""小于"或"等于")反应物能量总和
(2)若2mol氢气完全燃烧生成水蒸气,则放出的热量__________(填">""<"或"=")570kJ。
(3)现有25°C、1.013×105Pa下的H2和CH4的混合气体0.5mol,完全燃烧生成一定质量的CO2气体和10.8g H2O(l),放出203kJ的热量,则1mol CH4完全燃烧生成CO2气体和H2O(l)放出的热量为__________kJ。
(4)美国阿波罗宇宙飞船上使用了一种新型电池装置,其构造如图所示,A、B两个电极均由多孔的炭块组成。该电池的正极反应式为:__________
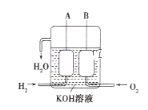
若该电池工作时增加了1mol H2O,电路中转移电子的物质的量为__________
(5)如果将上述装置中通入的氢气改成CH4气体,也可以组成一个原电池装置,电池的总反应方程式为:CH4+2O2+2KOH==K2CO3+3H2O,则该电池的负极反应式为:__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚石和石墨是碳元素的两种同素异形体,在100 kPa时,1 mol石墨转化为金刚石,要吸收1.895 kJ的热量.试判断在100 kPa压强下,下列结论正确的是( )
A.石墨比金刚石稳定
B.金刚石比石墨稳定
C.1 mol石墨比1 mol金刚石的总能量高
D.石墨转化为金刚石是物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,所选装置或实验设计合理的是
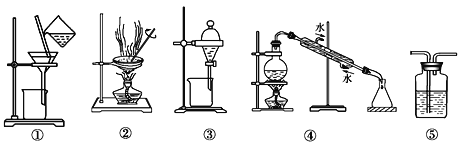
A. 图⑤所示装置中盛有饱和Na2SO3溶液除去SO2中含有的少量HCl
B. 用乙醇提取碘水中的碘选择图③所示装置
C. 用图①和②所示装置进行粗盐提纯
D. 用图④所示装置进行石油分馏实验制取汽油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值。下列有关叙述正确的是
A. 1L 0.1 mol·L-1CH3COOH溶液中含H+的数目为0.1NA
B. 标准状况下.2.24LCl2溶于水,转移的电子数为0.1NA
C. 100g质量分数为46%的酒精溶液中含氧原子总数为4NA
D. 常温下,将1molFe加入足量硝酸中,生成H2的分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Mg、Al、Fe 三种金属粉末状混合物中,加人过量盐酸充分反应,过滤后向滤液中加入过量NaOH溶液充分反应,再过滤后滤液中存在的离子有
A. Al3+ B. Cu2+ C. Mg2+ D. AlO2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.分散质微粒直径介于1~10 nm之间的分散系称为胶体
B.Fe(OH)3胶体是纯净物
C.利用丁达尔现象可以区别溶液与胶体
D.胶体微粒不能透过滤纸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学来源于生活又服务于生活,化工生产是指对原料进行化学加工,最终获得有价值的产品的生产过程。某研究小组利用含硫酸亚铁和硫酸铜的工业废料制备铁红(氧化铁)和硫酸铵晶体。流程如下:
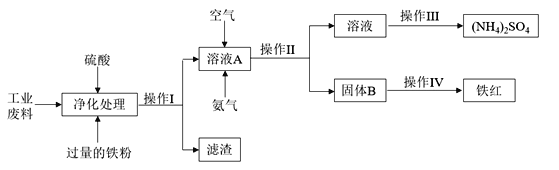
请回答下列问题:
(1)操作I的名称________________,滤渣的成分为__________________。
(2)简述下列实验操作:
①检验溶液A中金属阳离子的方法为____________________________________________________;
②检验固体B是否洗涤干净的方法是____________________________________________________。
(3)请写出溶液A中反应的离子方程式_______________________________________________________
(4) 测定废料中硫酸铜的质量分数:称取a g废料样品,将操作I得到的滤渣用足量的稀硫酸溶解、过滤、洗涤、干燥,称得固体的质量为b g,则废料中硫酸铜的质量分数为_______________(写出表达式。)
(5) 某同学提出另一种制备铁红的方法:往工业废水中加入足量的硫酸和双氧水,通过下列操作也可以得到铁红,请配平下列离子方程式_____ Fe2++ _____ H2O2 + _____ H+= _____ Fe3+ + ____ H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com