
 图中,A、B、C、D、E是常见单质,其中B、C、E为金属.G、H、I、F是B、C、D、E分别和A形成的化合物,G物质有磁性.
图中,A、B、C、D、E是常见单质,其中B、C、E为金属.G、H、I、F是B、C、D、E分别和A形成的化合物,G物质有磁性.
| ||
| ||
| ||
| ||
| ||
| ||
| ||
| ||


 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
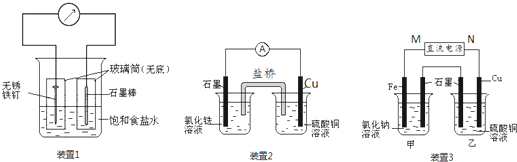
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 第一电离能 | 电负性 | 气态氢化物稳定性 | 酸性 |
| N | C | H2S | H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
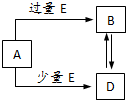 已知A、B、D、E均为中学化学中的常见物质,它们之间的转化关系如图所示(部分产物略去),则下列有关物质的推断不正确的是( )
已知A、B、D、E均为中学化学中的常见物质,它们之间的转化关系如图所示(部分产物略去),则下列有关物质的推断不正确的是( )| A、若A是铁,则E可能为稀硝酸 |
| B、若A是CuO,E是碳,则B为CO |
| C、若A是AlCl3溶液,E可能是氨水 |
| D、若A是NaOH溶液,E是CO2,则B为NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、B的物质的量浓度 |
| B、混合气体的密度 |
| C、混合气体的平均相对分子质量 |
| D、混合气体的压强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com