
| A. | 2.60g | B. | 3.90g | C. | 6.50g | D. | 13.65g |
分析 完全反应后滤液中没有Cu2+,且有剩余固体,说明溶液中也没有Fe3+,则溶液中阳离子有Zn2+、Fe2+和H+,溶质为ZnCl2、FeCl2和HCl,
根据电荷守恒得2n(Fe2+)+2n(Zn2+)+n(H+)=n(Cl-),则n(Zn2+)+n(Fe2+)=$\frac{4.40mol/L×0.1L-0.40mol/L×0.2L}{2}$mol=0.18mol,生成n(H2)=$\frac{0.896L}{22.4L/mol}$=0.04mol,因为盐酸有剩余,溶液残留固体是Cu,n(Cu)=$\frac{1.28g}{64g/mol}$=0.02mol,
设Zn的物质的量为xmol、Fe2O3的物质的量为ymol,根据原子守恒得:x+2y=0.18,根据转移电子守恒得:2x=0.04×2+0.02×2+2y×1,据此计算出锌的物质的量,再根据m=nM计算Zn的质量.
解答 解:完全反应后滤液中没有Cu2+,反应后有残留固体,则溶液中也没有Fe3+,则溶液中阳离子有Zn2+、Fe2+和H+,溶质为ZnCl2、FeCl2和HCl,
根据电荷守恒得2n(Fe2+)+2n(Zn2+)+n(H+)=n(Cl-),则n(Zn2+)+n(Fe2+)=$\frac{4.40mol/L×0.1L-0.40mol/L×0.2L}{2}$mol=0.18mol,
反应生成氢气的物质的量为:n(H2)=$\frac{0.896L}{22.4L/mol}$=0.04mol,
因为盐酸有剩余,溶液残留固体是Cu,其物质的量为:n(Cu)=$\frac{1.28g}{64g/mol}$=0.02mol,
设Zn的物质的量为xmol、Fe2O3的物质的量为ymol,
根据原子守恒得:①x+2y=0.18,
根据转移电子守恒得:②2x=0.04×2+0.02×2+2y×1,
联立①②解得:x=0.10、y=0.04,
所以m(Zn)=0.10mol×65g/mol=6.5g,
故选C.
点评 本题考查混合物反应的计算,侧重考查分析计算能力,题目难度中等,明确溶液中的溶质是解本题关键,根据原子守恒、转移电子守恒进行计算,能化繁为简,提高效率.


科目:高中化学 来源: 题型:选择题
| A. | 氧化性(酸性溶液):Co(OH)3>FeCl3>I2 | B. | 还原性(碱性溶液):I2>Fe(OH)2>KIO3 | ||
| C. | 热稳定性:NaCl>NaClO4>NaClO | D. | 酸性(水溶液):HSCN>H2CO3>HCN |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在Cu2O、Cu2S中Cu元素化合价都是+1价 | |
| B. | 反应中Cu元素被氧化,S元素被还原 | |
| C. | Cu2S在反应中既是氧化剂,又是还原剂 | |
| D. | 每生成6.4g Cu,反应中转移0.1 mole- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.24g | B. | 3.36g | C. | 5.60g | D. | 10.08g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
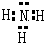 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2是硅酸的酸酐,但不能由SiO2直接制硅酸 | |
| B. | 二氧化硅是通讯材料光导纤维的主要原料 | |
| C. | 氧化铝陶瓷、碳化硅陶瓷都是重要的高温结构陶瓷 | |
| D. | 二氧化硅熔点与干冰相差不大,它们都是酸性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molNa2O2固体中含离子总数为4NA | |
| B. | 0.1mol/L的AgNO3溶液中,阳离子所带正电荷数目为0.1NA | |
| C. | 标准状况下,22.4LSO3所含分子数为NA | |
| D. | 23g钠在氧气中完全燃烧失电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na→Na2O2→NaOH→Na2CO3 | B. | Fe→FeCl2→Fe(OH)2→Fe(OH)3 | ||
| C. | Al→Al2O3→Al(OH)3→NaAlO2 | D. | Si→SiO2→Na2SiO3→H2SiO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com