
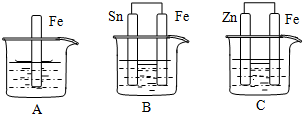
分析 (1)A中铁和稀硫酸发生化学腐蚀,生成硫酸亚铁和氢气;
(2)该装置构成原电池,Fe易失电子作负极、Sn作正极,正极上氢离子得电子发生还原反应而生成氢气;
(3)构成原电池的装置B、C将化学能转化成电能,伴随电流的产生;C装置中Zn易失电子作负极、Fe作正极,作负极的金属加速被腐蚀,作正极的金属被保护,金属腐蚀快慢速率:作负极的金属>发生化学腐蚀的金属>作正极的金属.
解答 解:(1)A中铁和稀硫酸发生化学腐蚀,生成硫酸亚铁和氢气,所以离子方程式为Fe+2H+=Fe2++H2↑,故答案为:Fe+2H+=Fe2++H2↑;
(2)该装置构成原电池,Fe易失电子作负极、Sn作正极,负极反应式为Fe-2e-=Fe2+,则铁溶解被腐蚀,正极上氢离子得电子发生还原反应而生成氢气,电极反应式为2H++2e-=H2↑,故答案为:Fe;2H++2e-=H2↑;
(3)构成原电池的装置B、C将化学能转化成电能,伴随电流的产生;C装置中Zn易失电子作负极、Fe作正极,作负极的金属加速被腐蚀,作正极的金属被保护,所以被腐蚀的金属是Zn,其电极反应式为Zn-2e-=Zn2+,金属腐蚀快慢速率:作负极的金属>发生化学腐蚀的金属>作正极的金属,所以铁被腐蚀快慢速率为B>A>C,
故答案为:BC;B>A>C.
点评 本题考查原电池原理,正确判断正负极并会书写电极反应式,知道金属被腐蚀快慢速率,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
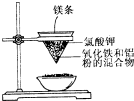 用如图所示的装置进行实验,回答下列问题:
用如图所示的装置进行实验,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 侯氏制碱法的主要原料是NaCl、CO2和NH3 | |
| B. | Na2CO3的热稳定性低于NaHCO3 | |
| C. | 该方法的副产物是NH4Cl | |
| D. | 母液可循环利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定不含I- | B. | 肯定含SO42- | C. | 肯定含有SO32- | D. | 肯定含有NH4+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com