
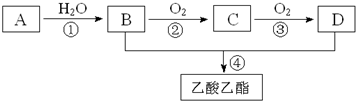
分析 A的产量可以用来衡量一个国家的石油化工发展水平,所以A是乙烯,中间产物C跟葡萄糖一样也能跟新制的Cu(OH)2发生反应产生砖红色沉淀,能和新制氢氧化铜悬浊液产生砖红色沉淀说明C含有醛基,所以C是乙醛,则B是乙醇;乙醇和D反应生成乙酸乙酯,所以D为乙酸.根据题目要求回答问题.
解答 解:(1)B为乙醇,结构简式为:CH3CH2OH,含官能团为羟基;D为乙酸,结构简式为:CH3COOH,含官能团羧基,
故答案为:羟基;羧基;
(2)乙烯和水生成乙醇的反应是加成反应,乙酸和乙醇生成乙酸乙酯的反应属于取代反应(或者酯化反应),
故答案为:加成反应;取代反应(或者酯化反应);
(4)乙烯和水在催化剂条件下发生加成反应生成乙醇,所以反应①的方程式为:CH2 =CH2+H2O$\stackrel{一定条件下}{→}$CH3CH2OH;
在铜或银作催化剂、加热条件下,乙醇被氧气氧化生成乙醛,所以反应②的方程式为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
在浓硫酸作催化剂、加热条件下,乙酸和乙醇反应酯化反应生成乙酸乙酯,所以反应④的方程式为:CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
点评 本题考查了有机物的推断,难度不大,正确推断A是解本题的关键,掌握基本有机反应类型.


科目:高中化学 来源: 题型:解答题
| 部分结构知识 | 部分性质 | |
| X | X的单质由双原子分子构成,分子中有14个电子 | X有多种氧化物,如XO、XO2、X2O4等;通常情况下XO2与X2O4共存 |
| Y | Y原子的次外层电子数等于最外层电子数的一半 | Y能形成多种气态氢化物 |
| Z | Z原子的最外层电子数多于4 | Z元素的最高正化合价与最低负化合价代数和等于6 |
| W | W原子的最外层电子数等于2n-3 (n为原子核外电子层数) | 化学反应中W原子易失去最外层电子形成Wn+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将Ba(OH)2•8H2O晶体与NH4Cl晶体混合搅拌,有氨气放出 | |
| B. | 甲烷燃烧 | |
| C. | 锌与稀硫酸反应产生H2 | |
| D. | 稀硫酸和NaOH的中和反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将少量SO2通入Ca(ClO)2溶液:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| B. | NaHCO3溶液中滴入少量澄清石灰水:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| C. | 用氨水吸收过量二氧化硫:NH3•H2O+SO2=NH4++HSO3- | |
| D. | Na2CO3溶液中通入CO2:H2O+CO2+CO32-═HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
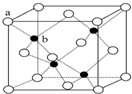 已知A、B、C、D、E、F、G为前四周期七种元素且原子序数依次增大,其中A的基态原子中没有成对电子,B的基态原子中有6种不同运动状态的电子,C原子核外成对电子数比未成对电子数多1,其氢化物常用作制冷剂,D原子中有2个未成对电子,E基态原子在同周期中原子半径最大,F原子价电子排布为nsn-1nPn+1,G基态原子核外所有轨道都处于全满状态且属ds区的元素.
已知A、B、C、D、E、F、G为前四周期七种元素且原子序数依次增大,其中A的基态原子中没有成对电子,B的基态原子中有6种不同运动状态的电子,C原子核外成对电子数比未成对电子数多1,其氢化物常用作制冷剂,D原子中有2个未成对电子,E基态原子在同周期中原子半径最大,F原子价电子排布为nsn-1nPn+1,G基态原子核外所有轨道都处于全满状态且属ds区的元素.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com