
| 1 |
| 2 |
| 3 |
| 2 |
| A、Mg(OH)2和Al(OH)3高温下不分解,所以可做工业阻燃剂 |
| B、等质量Mg(OH)2和Al(OH)3相比,Mg(OH)2阻燃效果较好 |
| C、Mg(OH)2比Al(OH)3热稳定性高 |
| D、Mg(OH)2和Al(OH)3作为工业阻燃剂与它们分解吸热及生成物具有耐高温性有关 |


科目:高中化学 来源: 题型:
| A、摩尔是国际单位制中的七个物理量之一 |
| B、摩尔表示物质的量 |
| C、1mol任何物质都含有6.02×1023个原子 |
| D、1mol O2中有6.02×1023个氧分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、12C、13C、14C 为碳元素的三种核素.元素周期表中碳的相对原子质量为12.01,说明自然界中的碳主要以12C的核素形式存在.14C为放射性核素,可用于同位素示踪 |
| B、汽车尾气催化转化装置可将尾气中的NO和CO等有害气体转化为N2和CO2,该装置中的催化剂可降低NO和CO反应的活化能,有利于提高该反应的平衡转化率 |
| C、能量是可以互相转化的.植物的光合作用可将太阳能转变成化学能,单晶硅可将光能转变成电能.原电池和电解池可实现化学能和电能的相互转化 |
| D、乳酸分子中既有羟基又有羧基,因此可在一定条件下缩聚得到聚乳酸(PLA).该高分子化合物是一种可降解的环保材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
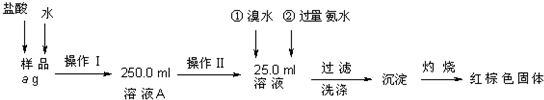
查看答案和解析>>
科目:高中化学 来源: 题型:
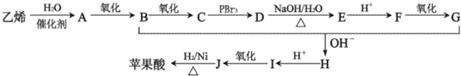
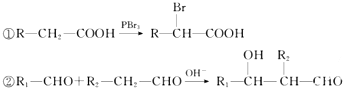
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
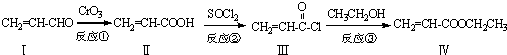
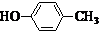 也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为
也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com