
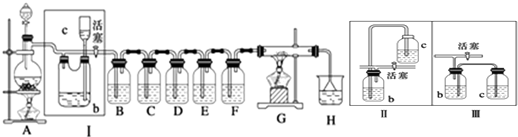
·ÖĪö £Ø1£©AŹĒĀČĘųµÄÖʱø×°ÖĆ£¬·¢Éś·“Ó¦ĪŖ£ŗ¶žŃõ»ÆĆĢÓėÅØŃĪĖįŌŚ¼ÓČČĢõ¼žĻĀÉś³ÉĀČ»ÆĆĢ”¢ĀČĘųŗĶĖ®£»
£Ø2£©¢ņÓė¢ńŌĄķĻąĶ¬£¬¶ų¢óÖŠŅņcĘææŚĆÜ·ā£¬²»ÄÜĘųĢåĮ÷ĶØ£»
£Ø3£©äå»ÆŃĒĢśČÜŅŗŃõ»ÆŃĒĢśĄė×ÓŗĶäåĄė×ÓĪŖĢśĄė×Ó£¬ČÜŅŗÓÉĒ³ĀĢÉ«±äĪŖÉīŗģ×ŲÉ«£»ĶØČėE»ģÓŠ¶žŃõ»ÆĮņµÄĀČ»Æ±µČÜŅŗ£¬Ńõ»Æ¶žŃõ»ÆĮņĪŖĮņĖį£¬Éś³É°×É«³Įµķ£»
£Ø4£©ŅĄ¾ŻG×°ÖƵÄÓ²ÖŹ²£Į§¹ÜÄŚŹ¢ÓŠĢ¼·Ū£¬·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬Ęä²śĪļĪŖ¶žŃõ»ÆĢ¼ŗĶĀČ»ÆĒā£¬½įŗĻŌ×ÓŹŲŗ抓³ö£»FĪŖGĢį¹©Ė®ÕōĘų£®
½ā“š ½ā£»£Ø1£©¶žŃõ»ÆĆĢÓėÅØŃĪĖįŌŚ¼ÓČČĢõ¼žĻĀÉś³ÉĀČ»ÆĆĢ”¢ĀČĘųŗĶĖ®£¬Ąė×Ó·½³ĢŹ½£ŗMnO2+4H++2Cl$\frac{\underline{\;\;”÷\;\;}}{\;}$Mn2++Cl2”ü+2H2O£»
¹Ź“š°øĪŖ£ŗMnO2+4H++2Cl$\frac{\underline{\;\;”÷\;\;}}{\;}$Mn2++Cl2”ü+2H2O£»
£Ø2£©¢ņÓė¢ńŌĄķĻąĶ¬£¬¶ų¢óÖŠŅņcĘææŚĆÜ·ā£¬²»ÄÜĘųĢåĮ÷ĶØ£»
¹Ź“š°øĪŖ£ŗ¢ņæÉŠŠ£¬¢ó²»ŠŠ£®¢ņÓė¢ńŌĄķĻąĶ¬£¬¶ų¢óÖŠŅņcĘææŚĆÜ·ā£¬Ģå»ż²»ÄÜøı䣬Ōö“óŃ¹Ēæ»įÓŠĪ£ĻÕ£»
£Ø3£©äå»ÆŃĒĢśČÜŅŗŃõ»ÆŃĒĢśĄė×ÓŗĶäåĄė×ÓĪŖĢśĄė×Ó£¬ČÜŅŗÓÉĒ³ĀĢÉ«±äĪŖÉīŗģ×ŲÉ«£»ĶØČėE»ģÓŠ¶žŃõ»ÆĮņµÄĀČ»Æ±µČÜŅŗ£¬Ńõ»Æ¶žŃõ»ÆĮņĪŖĮņĖį£¬Éś³É°×É«³Įµķ£»
¹Ź“š°øĪŖ£ŗČÜŅŗÓÉĒ³ĀĢÉ«±äĪŖÉīŗģ×ŲÉ«£»Éś³É°×É«³Įµķ£»
£Ø4£©G×°ÖƵÄÓ²ÖŹ²£Į§¹ÜÄŚŹ¢ÓŠĢ¼·Ū£¬·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬Ęä²śĪļĪŖ¶žŃõ»ÆĢ¼ŗĶĀČ»ÆĒā£¬½įŗĻŌ×ÓŹŲŗ抓³ö»Æѧ·½³ĢŹ½ĪŖ£ŗC+2H2O+2Cl2ØTCO2”ü+4HCl”ü£»FĪŖGĢį¹©Ė®ÕōĘųµÄ×÷ÓĆ£»
¹Ź“š°øĪŖ£ŗC+2H2O+2Cl2ØTCO2”ü+4HCl”ü£»ĻņGÖŠĢį¹©·“Ó¦ĖłŠčµÄĖ®ÕōĘų£®
µćĘĄ ±¾Ģāæ¼²éĮĖŹµŃéŹŅÖʱøĀČĘųµÄ·“Ó¦ŌĄķŗĶ×°ÖĆŃ”Ōń£¬ŹģĻ¤ĀČĘųÖʱøŌĄķŗĶĀČĘųµÄŠŌÖŹŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®


 æģĄÖŹī¼ŁŹī¼ŁÄÜĮ¦×Ō²āÖŠĪ÷Źé¾ÖĻµĮŠ“š°ø
æģĄÖŹī¼ŁŹī¼ŁÄÜĮ¦×Ō²āÖŠĪ÷Źé¾ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | FeSO4”¢Fe£ØNO3£©3£» Fe2£ØSO4£©3”¢HNO3”¢N2O”¢H2O | |
| B£® | HNO3”¢FeSO4£» Fe2£ØSO4£©3”¢Fe£ØNO3£©3”¢N2O”¢H2O | |
| C£® | HNO3”¢Fe2£ØSO4£©3£» FeSO4”¢Fe£ØNO3£©3”¢N2O”¢H2O | |
| D£® | Fe2£ØSO4£©3”¢N2O£» FeSO4”¢HNO3”¢Fe£ØNO3£©3”¢H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŹµŃé¢ŁÖŠ²śÉśµÄĘųĢåĪŖ°±Ęų£¬²¢æɵĆŌČÜŅŗÖŠc£ØNH4+£©=0.2 mol•L-1 | |
| B£® | ŹµŃé¢ŪÖŠµÄ°×É«³ĮµķÖŠŅ»¶ØÓŠBaSO4£¬ĪŽBaCO3 | |
| C£® | ŌČÜŅŗÖŠŅ»¶ØÓŠK+£¬ĒŅc£ØK+£©=0.4 mol•L-1 | |
| D£® | ČōŅŖÅŠ¶ĻŌČÜŅŗÖŠŹĒ·ńÓŠCl-£¬ĪŽŠčĮķĶāÉč¼ĘŹµŃéŃéÖ¤ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
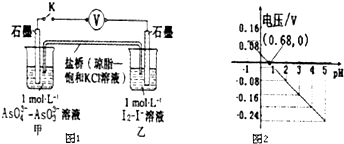
| A£® | µ÷½ŚpHæÉŅŌøı䷓ӦµÄ·½Ļņ | |
| B£® | pH=0.68 Ź±£¬·“Ó¦“¦ÓŚĘ½ŗāדĢ¬ | |
| C£® | pH=5 Ź±£¬øŗ¼«µē¼«·“Ó¦Ź½ĪŖ2I--2e-ØTI2 | |
| D£® | pH£¾0.68Ź±£¬Ńõ»ÆŠŌI2£¾AsO${\;}_{4}^{3-}$ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆŠ”ĖÕ“ņÖĪĮĘĪøĖį¹ż¶ą2H++CO32-ØTCO2”ü+H2O | |
| B£® | ÓĆĒāŃõ»ÆÄĘČÜŅŗ³żČ„ĀĮ±ķĆęµÄŃõ»ÆĤ Al2O3+2OH-ØT2AlO2-+H2O | |
| C£® | ĀČ»ÆŃĒĢśČÜŅŗĶØČėĀČĘų Fe2++Cl2ØTFe3++2Cl- | |
| D£® | ÓĆŹ³“׳żČ„Ė®ĘæÖŠµÄĖ®¹ø CO32-+2H+ØTH2O+CO2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ijŠĖȤŠ”×éĶ¬Ń§ĄūÓĆŃõ»Æ»¹Ō·“Ó¦£ŗ2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2£ØSO4£©3+K2SO4+8H2OÉč¼ĘČēĻĀŌµē³Ų£¬ŃĪĒÅ֊װӊ±„ŗĶČÜŅŗ£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
ijŠĖȤŠ”×éĶ¬Ń§ĄūÓĆŃõ»Æ»¹Ō·“Ó¦£ŗ2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2£ØSO4£©3+K2SO4+8H2OÉč¼ĘČēĻĀŌµē³Ų£¬ŃĪĒÅ֊װӊ±„ŗĶČÜŅŗ£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | aµē¼«ÉĻ·¢ÉśµÄ·“Ó¦ĪŖ£ŗMnO4-+8H++5e-ØTMn2++4H2O | |
| B£® | ĶāµēĀ·µē×ÓµÄĮ÷ĻņŹĒ“Óaµ½b | |
| C£® | µē³Ų¹¤×÷Ź±£¬ŃĪĒÅÖŠµÄSO42-ŅĘĻņ¼×ÉÕ± | |
| D£® | bµē¼«ÉĻ·¢Éś»¹Ō·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | $\frac{3}{£Øm-n£©}$mL | B£® | $\frac{£Øm-n£©}{3}$ mL | C£® | $\frac{£Ø4m-1£©}{13}$ mL | D£® | $\frac{£Øm-n£©}{3}$3 mL |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | K+”¢Cl-”¢NO3-”¢Ag+ | B£® | H+”¢HCO3-”¢Na+”¢Cl- | ||
| C£® | Na+”¢OH-”¢Ba2+”¢CO32- | D£® | Mg2+”¢Cl-”¢H+”¢SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚ0.1molNaHSO4¾§ĢåÖŠŃōĄė×ÓÓėŅõĄė×Ó×ÜŹżĪŖ0.3NA | |
| B£® | 1.0L0.1mol•L-1NH4NO3ČÜŅŗÖŠŗ¬ÓŠµÄļ§øłĄė×ÓŹżŹĒ0.1”Į6.02”Į1023 | |
| C£® | 7.8gNa2O2Óė×ćĮæCO2·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ0.1NA | |
| D£® | Ļņ½öŗ¬0.2molFeI2µÄČÜŅŗÖŠ³ÖŠųĶØČėĀČĘų£¬µ±ÓŠ0.1molFe2+±»Ńõ»ÆŹ±£¬ŠčĶØČė±źæöĻĀC121.12L |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com