
【题目】某原电池装置如图所示,电池总反应为:2Ag+Cl2===2AgCl。下列说法正确的是

A. 正极反应为AgCl+e-===Ag+Cl-
B. 放电时,交换膜右侧溶液中有大量白色沉淀生成
C. 当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
D. 若用NaCl溶液代替盐酸,则电池总反应随之改变
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. P4和CH4都是正四面体分子且键角都为109o28ˊ
B. H2O是一种非常稳定的化合物,这是由于氢键所致
C. NO3-和CO32-是等电子体,均为平面正三角形结构
D. 金属晶体与熔融态的离子晶体导电都是物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不导热的恒容密闭容器中通入CO(g)和H2O(g),一定条件下使反应CO(g)+H2O(g) ![]() CO2(g)+H2(g)达到平衡状态,正反应速率随时间变化的示意图如下所示。由图可得出的正确结论是
CO2(g)+H2(g)达到平衡状态,正反应速率随时间变化的示意图如下所示。由图可得出的正确结论是
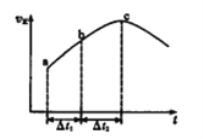
A. 反应物浓度:a点小于c点
B. c点时反应进行的程度最大
C. 该反应的正反应为吸热反应
D. △t1=△t2时,生成H2的物质的量:a~b段小于b~c段
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备H2和Cl2通常采用下列反应:
Zn+H2SO4===ZnSO4+H2↑
MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
据此,从下列所给仪器装置中选择制备并收集H2的装置______(填代号)和制备并收集干燥、纯净Cl2的装置______(填代号)。
可选用制备气体的装置:


查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向等物质的量浓度的HCl、AlCl3、NH4Cl、MgCl2混合溶液中逐滴加入1 mol·L-1的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。下列有关说法正确的是( )

A.在O~a段加入的NaOH溶液与NH4Cl反应
B.在b~c段加入NaOH溶液发生反应的离子方程式为Al3++3OH-===Al(OH)3↓
C.在d~e段加入NaOH溶液发生反应的离子方程式为Al3++4OH-===AlO![]() +2H2O
+2H2O
D.在滴加NaOH溶液全过程中主要微粒参与反应的先后顺序是H+、Al3+、Mg2+、NH![]() 、Al(OH)3
、Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下说法正确的是( )
A.物质所含元素化合价升高的反应叫还原反应
B.在氧化还原反应中,失去电子的元素化合价降低
C.物质中某元素失去电子,则此物质是氧化剂
D.还原剂中必定有一种元素被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)Ⅰ.1100 ℃时,体积为2L的恒容容器中发生如下反应:Na2SO4(s)+4H2 (g)![]() Na2S(s)+4H2O(g)
Na2S(s)+4H2O(g)
(1)下列能判断反应达到平衡状态的是________。
A.容器内气体压强不再变化
B.H2的体积分数不再变化
C.1 mol H-H键断裂同时2 mol H-O键形成
D.Na2S的质量不再变化
E.υ(正)=υ(逆)
F.容器内气体密度不再变化
(2)若2 min时反应达平衡,此时气体质量增加8 g,则用H2表示该反应的反应速率为: 。
Ⅱ.丙烷燃料电池,以KOH溶液为电解质溶液。
(3)通入丙烷的电极为_____(填“正极”或“负极”),正极的电极反应式为 。
(4)燃料电池的优点________。
(5)若开始时电解质溶液中含KOH的物质的量为0.25 mol,当溶液中K2CO3的物质的量为0.1 mol时,消耗标准状况下丙烷的体积为 mL(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于铁及其化合物的说法正确的是
A.赤铁矿的主要成分是Fe3O4
B.除去FeCl2 溶液中的FeCl3杂质可以向溶液中加锌粉,然后过滤
C.磁铁矿粉末溶于盐酸后,加入KSCN溶液,溶液变红色
D.Fe3O4俗称铁红
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是 ( )
A.钠和冷水反应 Na+2H2O=Na++2OH+H2↑
B.金属铝溶于氢氧化钠溶液 Al+2OH=AlO2+H2
C.铁锈溶于盐酸中:Fe2O3+6H+=2 Fe 3++3H2↑
D.铁跟稀硫酸反应:Fe+2H+=Fe2++H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com