
【题目】氢气既是一种优质的能源,又是一种重要化工原料,高纯氢的制备是目前的研究热点。
(1)甲烷水蒸气催化重整是制备高纯氢的方法之一,甲烷和水蒸气反应的热化学方程式是:
CH2(g)+2H2O(g)![]() CO2(g)+4H2(g) △H=+165.0kJ·mol-1
CO2(g)+4H2(g) △H=+165.0kJ·mol-1
已知反应器中存在如下反应过程:
I.CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H1=+206.4kJ·mol-1
CO(g)+3H2(g) △H1=+206.4kJ·mol-1
II.CO(g)+H2O(g)![]() CO2(g)+H2(g) △H2
CO2(g)+H2(g) △H2

根据上述信息计算:a=___、△H2=___。
(2)某温度下,4molH2O和lmolCH4在体积为2L的刚性容器内同时发生I、II反应,达平衡时,体系中n(CO)=bmol、n(CO2)=dmol,则该温度下反应I的平衡常数K值为___(用字母表示)。
(3)欲增大CH4转化为H2的平衡转化率,可采取的措施有___(填标号)。
A.适当增大反应物投料比武n(H2O):n(CH4)
B.提高压强
C.分离出CO2
(4)H2用于工业合成氨:N2+3H2![]() 2NH3。将n(N2):n(H2)=1:3的混合气体,匀速通过装有催化剂的反应器反应,反应器温度变化与从反应器排出气体中NH3的体积分数φ(NH3)关系如图,反应器温度升高NH3的体积分数φ(NH3)先增大后减小的原因是___。
2NH3。将n(N2):n(H2)=1:3的混合气体,匀速通过装有催化剂的反应器反应,反应器温度变化与从反应器排出气体中NH3的体积分数φ(NH3)关系如图,反应器温度升高NH3的体积分数φ(NH3)先增大后减小的原因是___。

某温度下,n(N2):n(H2)=1:3的混合气体在刚性容器内发生反应,起始气体总压为2×l07Pa,平衡时总压为开始的90%,则H2的转化率为___,气体分压(p分)=气体总压(p总)×体积分数,用某物质的平衡分压代替物质的量浓度也可以表示化学平衡常数(记作Kp),此温度下,该反应的化学平衡常数Kp=___(分压列计算式、不化简)。
【答案】415.1 -41.4kJ·mol-1 ![]() AC 温度低于T0时未达平衡,温度升高、反应速率加快,NH3的体积分数增大;高于T0时反应达平衡,由于该反应是放热反应,温度升高平衡常数减小,NH3的体积分数减小 20%
AC 温度低于T0时未达平衡,温度升高、反应速率加快,NH3的体积分数增大;高于T0时反应达平衡,由于该反应是放热反应,温度升高平衡常数减小,NH3的体积分数减小 20% 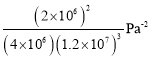
【解析】
(1)根据△H1=反应物键能-生成物键能计算a;根据盖斯定律计算△H2;
(2)根据K=![]() 计算;
计算;
(3)欲增大CH4转化为H2的平衡转化率要使平衡正向移动;
(4)温度低于T0时未达平衡,高于T0时反应达平衡,该反应是放热反应;根据压强比等于气体物质的量之比进行计算;
(1)反应CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H1==4a kJ·mol-1+2×465 kJ·mol-1-(1076 kJ·mol-1+3×436 kJ·mol-1)= +206.4kJ·mol-1,解得a=415.1 kJ·mol-1;ⅢCH2(g)+2H2O(g)
CO(g)+3H2(g) △H1==4a kJ·mol-1+2×465 kJ·mol-1-(1076 kJ·mol-1+3×436 kJ·mol-1)= +206.4kJ·mol-1,解得a=415.1 kJ·mol-1;ⅢCH2(g)+2H2O(g)![]() CO2(g)+4H2(g) △H=+165.0kJ·mol-1,I.CH4(g)+H2O(g)
CO2(g)+4H2(g) △H=+165.0kJ·mol-1,I.CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H1=+206.4kJ·mol-1,根据盖斯定律可知II=Ⅲ- I,所以△H2=△H-△H1=+165.0kJ·mol-1-206.4kJ·mol-1=-41.4kJ·mol-1,
CO(g)+3H2(g) △H1=+206.4kJ·mol-1,根据盖斯定律可知II=Ⅲ- I,所以△H2=△H-△H1=+165.0kJ·mol-1-206.4kJ·mol-1=-41.4kJ·mol-1,
故答案为:415.1;-41.4kJ·mol-1;
(2)由n(CO2)=dmol可知反应II生成的n(H2)= dmol,同时消耗的n(CO)=dmol,消耗的n(H2O)=dmol,则在反应I中生成的n(CO)=(b+d)mol,消耗的n(CH4)= (b+d)mol,消耗的n(H2O)= (b+d)mol,生成的n(H2)=(3b+3d)mol,则平衡时体系内:n(CH4)=(1-b-d)mol、n(H2O)=(4-b-2d)mol、n(CO)=bmol、n(H2)=(3b+4d)mol,容器体积为2L,故平衡常数 ,
,
故答案为:![]() ;
;
(3)A.适当增大反应物投料比武n(H2O):n(CH4),增大水的量促进甲烷转化成CO,促进CO转化成CO2,故A正确;
B.提高压强,反应I平衡左移,故B错误;
C.分离出CO2可使平衡右移,故C正确;
故答案为:AC;
(4)温度低于T0时未达平衡,温度升高、反应速率加快,NH3的体积分数增大;高于T0时反应达平衡,由于该反应是放热反应,温度升高平衡常数减小,NH3的体积分数减小;
设初始加入的N2为1 mol、H2为3 mol ,温度、体积一定时气体物质的量之比等于压强之比,气体物质的量减少4×10 % =0.4 mol;

其中p0=2×l07Pa ;
H2的转化率为0.6/3=20%;
平衡常数
故答案为:温度低于T0时未达平衡,温度升高、反应速率加快,NH3的体积分数增大;高于T0时反应达平衡,由于该反应是放热反应,温度升高平衡常数减小,NH3的体积分数减小;20%;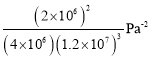 。
。


科目:高中化学 来源: 题型:
【题目】探究苯与溴反应生成溴苯的实验可用如图所示装置,分析装置并完成下列题目:
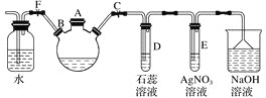
(1)关闭止水夹F,打开止水夹C,由A口向装有少量苯的三口烧瓶中加入过量液溴,再加入少量铁屑,塞住A口,则三口烧瓶中发生反应的有机化学方程式为______________________。
(2)D、E试管内出现的现象分别为:D.______, E.__________。
(3)待三口烧瓶中的反应进行到仍有气泡冒出时,松开止水夹F,关闭止水夹C,可以看到的现象是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁、铝、铁是三种重要金属,它们的单质和化合物应用十分广泛。回答下列问题:
(1)镁、铝第一电离能大小的关系是I1(Mg)___I1(Al),金属镁、铝熔点大小关系是Mg___Al。(填“大于”、“等于”或“小于”)
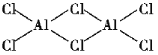
(2)氯化铝加热时易升华,实验测得铝元素与氯元素形成化合物的实际组成为Al2Cl6,其结构简式如图所示。其中处于中间的Cl原子杂化轨道类型为___杂化,分子中所有原子___(能、不能)在同一平面上。
(3)硝酸铁和尿素在乙醇中生成[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁]。产物是一种重要的配合物,用作有机铁肥,简称铁氮肥。基态Fe3+的核外电子排布式为___。尿素分子中σ键与π键的数目之比为___。NO3-的空间构型为___,经测定N2O5晶体中存在NO2+和NO3-,NO2+中氮原子为___杂化。
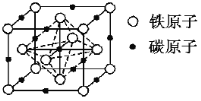
(4)碳溶解在γ-Fe中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构如图所示。晶体中与相邻铁原子距离相等且最近的铁原子有___个,该物质的化学式为___。若晶体密度为dg·cm-3,则晶胞中最近的两个碳原子的距离为___pm(阿伏加德罗常数的值为NA表示,写出简化后的计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。
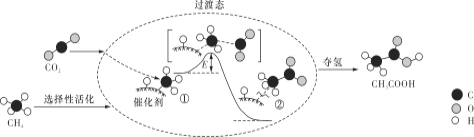
下列说法不正确的是
A. 生成CH3COOH总反应的原子利用率为100%
B. CH4→CH3COOH过程中,有C―H键发生断裂
C. ①→②放出能量并形成了C―C键
D. 该催化剂可有效提高反应物的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验能达到实验目的的是( )

A.用甲装置从KI和I2的固体混合物中回收I2
B.用乙装置接收石油分馏实验中所得的馏分
C.用丙装置测量用MnO2和浓盐酸共热制得的Cl2体积
D.用丁装置准确量取一定体积的KMnO4标准溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔在Pd表面选择加氢的反应机理如图所示。其中吸附在Pd表面上的物种用*标注。
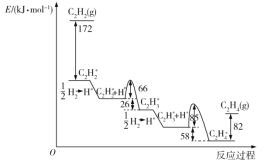
下列有关说法正确的是( )
A.该正反应历程中最大能垒(活化能)为85kJ·mol-1
B.吸附反应为吸热反应
C.Pd为固体催化剂,其表面积大小对催化效果无影响
D.C2H2*+H*→C2H3*只有化学键的形成过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作和现象与结论对应关系正确的是![]()
选项 | 实验操作 | 实验现象 | 结论 |
A | 测量等浓度的 |
|
|
B | 将 | 溴水褪色 |
|
C | 取少量的变质 | 酸性高锰酸钾溶液褪色 |
|
D | 向苯酚的苯溶液中加入足量NaOH溶液,振荡静置 | 分层 | 上层为苯,下层为NaOH与苯酚钠的混合溶液 |
A.AB.BC.CD.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不能用勒夏特列原理解释的是( )
A.对于CO(g)+NO2(g)![]() CO2(g)+NO(g)的平衡体系,增大压强可使颜色变深
CO2(g)+NO(g)的平衡体系,增大压强可使颜色变深
B.氢气和氮气合成氨的反应中,在加压下有利于氨的生成
C.开启可乐瓶,瓶中马上泛起大量气泡
D.利用排液法收集氯气时常用液体为饱和食盐水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2—CaO作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛。下列说法中不正确的是( )

A.由TiO2制得1mol金属Ti,理论上外电路转移4mol电子
B.阳极的电极反应式为C+2O2--4e-=CO2↑
C.在制备金属钛前后,整套装置中CaO的总量会不断减少
D.装置中石墨电极材料需要定期更换
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com