
【题目】在有机物分子中,若某个碳原子连接4个不同的原子或原子团,则这种碳原子称为“手性碳原子”,凡有一个手性碳原子的物质一定具有光学活性。已知某有机物结构如下:具有光学活性,当它发生下列反应后生成的有机物仍然具光学活性的是
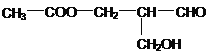
A. 与NaOH溶液共热 B. 与甲酸发生酯化反应
C. 与氧气发生催化氧化 D. 在催化剂存在下与H2作用
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:
【题目】下列实验中,分离提纯的方法不正确的是( )
选项 | 实验 | 分离、提纯方法 |
A | 提纯粗苯甲酸 | 重结晶 |
B | 分离乙醇和丁醇 | 蒸馏 |
C | 除去乙炔中的H2S气体 | 用CuSO4溶液洗气 |
D | 提纯硝基苯 | 碱洗分液-水洗分液-蒸馏 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,则下列叙述中正确的是
A. 1L0.5mol/L的H2SO4溶液中含有2NA个氧原子
B. 11.2LCH4气体完全燃烧可得0.5NA个CO2分子
C. 16g O2、O3混合气中含有8NA个电子
D. 标准状况下,11.2L水和0.5mol甲烷的质量比为9:8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是
A.化石燃料在任何条件下都能充分燃烧
B.化石燃料在燃烧过程中能产生污染环境的CO、SO2等有害气体
C.直接燃烧不如将煤进行深加工后再燃烧的效果好
D.固体煤变为气体燃料后,燃烧效率将更高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法错误的是
A. 硅可用于制造光导纤维
B. 铝槽车可用于浓硫酸的贮运
C. 铝热反应可用于焊接铁轨
D. 呈液态钠钾合金可用于快中子反应堆的热交换剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
Zn 在现代工业中对于电池制造有不可磨灭的地位,锌还是人体必需的微量元素之一,在人体生长发育、生殖遗传、免疫、内分泌等重要生理过程中起着极其重要的作用。
(l)元素Zn在周期表中的位置为_____,基态Zn原子的电子排布式为_____。
(2)在[Zn(NH3)4]2+中,Zn2+提供4s和4p共四个空轨道,与4个NH3分子形成_____键,Zn2+采取sp3杂化,预测[Zn(NH3)4]2+的空间构型为______。
(3)金属Zn晶体密置层采取…ABAB…方式堆积,其堆积方式名称为:______,配位数为:____。
(4)闪锌矿(ZnS )晶胞如图所示
白球为S2-离子、黑球为Zn2+离子,与Zn2+距离最近的四个S2-所围成的空间构型为_____,若晶胞参数为a,则Zn2+与S2-最近距离为______(用含a的代数式表示)。

(5)具有相似晶胞结构的ZnS和ZnO,ZnS熔点为1830℃,ZnO熔点为1975℃,后者较前者高是由于______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.质子核磁共振谱(PMR)是研究有机物结构的有力手段之一,在所研究的有机化合物分子中,每一结构中的等性氢原子在PMR谱中都给出了相应的峰(信号),谱中峰的强度与结构中的H原子数成正比。例如,乙醛的结构式为CH3CHO,其PMR谱中有两个信号,其强度之比为3∶1。分子式为C3H6O2的有机物,如果在PMR谱上观察到的氢原子给出的峰有两种情况 :
第一种情况峰给出的强度比为3∶3,请写出其对应化合物的结构简式__________________;
第二种情况峰的强度比为3∶2∶1,请写出该化合物的可能结构简式___________________、
_________________________、_________________________。
Ⅱ.胡萝卜中含有较多的胡萝卜素,它是人体的主要营养元素之一。已知α-胡萝卜素的键线式结构如下:

(1)写出α-胡萝卜素的分子式__________________。
(2)1 mol α-胡萝卜素最多能与__________________mol Br2反应。
(3)β-胡萝卜素与α-胡萝卜素互为同分异构体,且只是虚线框内部分不同,但碳的骨架相同,写出β-胡萝卜素方框内可能的结构简式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。一种制备草酸钴晶体(CoC2O4·2H2O)的工艺流程如下:

已知:①水钴矿主要成分为Co2O3、Co(OH)3,还含有少量Fe2O3、Al2O3、MnO等杂质。
②浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等。
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(金属离子浓度以0.01mol·L-1计)
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀pH | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1) 写出浸出过程中Co(OH)3发生反应的离子方程式:____________________。
(2) NaClO3的作用是_______________________。
(3) 加Na2CO3调pH的范围应该在_____之间。加入萃取剂的目的是____________。
(4) 在空气中加热5.49g草酸钴晶体(CoC2O4·2H2O)样品,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表:
温度范围/℃ | 固体质量/g |
150~210 | 4.41 |
290~320 | 2.41 |
890~920 | 2.25 |
经测定,210~290℃过程中产生的气体只有CO2,此过程发生反应的化学方程式是____________________。[M(CoC2O4·2H2O=183g/mol]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期金属元素甲~戊在周期表中的相对位置如右表所示,下面判断不正确的是( )
甲 | 乙 | |
丙 | 丁 | 戊 |
A. 原子半径: 丙>丁>戊 B. 金属性:甲<丙
C. 最外层电子数:甲>乙 D. 氢氧化物碱性:丙>丁>戊
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com