
【题目】阿司匹林是一种历史悠久的解热镇痛药,对预防血栓和脑梗有很好的作用,M是一种防晒剂,它们的结构简式分别为
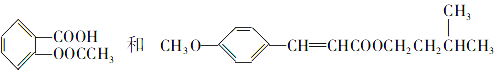 ,
,
它们的合成路线如下:

已知:Ⅰ. E的俗称水杨酸,学名2-羟基苯甲酸

IV.苯的同系物与氯气的反应遵循“催化在苯环,光照在侧链”。
根据以上信息回答下列问题
(1)阿司匹林中官能团的名称为______
(2) B→D过程的反应类型为______请写出C和I的结构简式________________
(3)由E→F的过程是缩聚反应,该过程化学方程式为_________
(4)下列关于阿司匹林和防晒剂M说法正确的是_________(双选)
A.M的分子式是C15H20O3
B.其中阿司匹林不能发生氧化反应
C.1mol阿司匹林完全水解,需消耗2molNaOH
D.1molM与足量氢气发生加成反应,最多消耗4molH2
(5)阿司匹林有多种同分异构体,请写出同时满足下列条件的任意一种同分异构体的结构简式________
ⅰ.苯环上有2个取代基;
ⅱ.能发生水解反应,能发生银镜反应,还能与NaHCO3产生CO2
iii.核磁共振氢谱有5组峰,峰面积之比为1:1:2:2:2
(6)写出由I到M的合成路线(第一步已给出):合成路线示例如下:
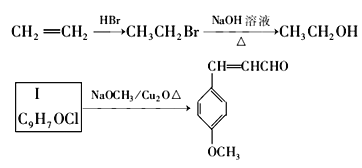 __________________________
__________________________
【答案】 羧基和酯基 取代 ![]() ,
,![]()
 AD
AD 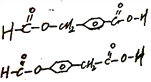

【解析】(1).-COOH为 羧基和-OOR’为酯基;
(2).B到D,由Cl取代H原子,为取代反应;由已知得A中含有苯环,则结构比为甲苯,由M的结构可得,C与I为对位官能团,即C为![]() ,H为-OH将甲基上的两个H取代,由已知ⅡⅢ得:I为Cl-苯环-CH=CH-CHO。
,H为-OH将甲基上的两个H取代,由已知ⅡⅢ得:I为Cl-苯环-CH=CH-CHO。
(3).Cl取代甲基上3个H,和临位苯环上1个H,后经催化4个Cl全部被-OH取代,由Ⅱ得,E为HOOC-苯环(临位)-OH,经脱水缩合的反应为: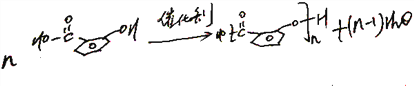
(4).A由已知得,A正确;B. 阿司匹林含有苯环,可以燃烧,即可以发生氧化反应,B错误;C. 阿司匹林水解产物水杨酸和乙酸,其中水杨酸含有酚羟基和羧基,则1mol该物质最多可与3mol NaOH发生反应,C错误;D. 苯环可与3mol氢气加成,碳碳双键可以使1mol氢气加成,D正确。故选择AD。
(5). 含有酯基、醛基、羧基,同时H原子由5种化学状态,所以要存在HCOOR-,苯环,-COOH,由于碳原子总数为8,则R为-CH2-,所以同分异构体可写为:HCOO-CH2-苯环-COOH。
(6).CH3-O-苯环-CH=CHCHO在加热条件下与Ag(NH3)2OH发生银镜反应,生成CH3-O-苯环-CH=CHCOONH3,再与酸反应生成CH3-O-苯环-CH=CHCOOH,与HOCH2CH2CH(CH3)2在热的浓硫酸作用下脱水合成M。


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ、下图是某同学设计的测定中和热的实验装置。

(1)强酸与强碱中和反应的实质,可用离子反应表示为________。 装置中使用碎泡沫塑料的目的是_________。
(2) 实验时,同学先分别在50mL烧杯中,各加入20mL 2mol/L的盐酸和20mL2mol/L的NaOH溶液,分别测其温度,分别测其温度的目的是________。
Ⅱ、某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:

(3)反应开始至2min,以气体Z表示的平均反应速率为_________.
(4)该反应的化学方程式为_________.
(5)若X、Y、Z均为气体,2min后反应达到平衡,反应达平衡时:此时体系的压强是开始时的_________倍;达平衡时,容器内混合气体的平均相对分子质量比起始投料时_________(填"增大""减小"或"相等").
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用废铅蓄电池填料(主要成分为PbO2、PbO、PbSO4等)作阴极,采取固相直接电解法可提取金属Pb,其装置如图所示(已知:PbSO4+3OH-=HPbO2-+S042-+H2O)。下列说法中错误的是

A. b与外接电源的负极相连
B. PbO2放电时电极反应式为:PbO2+4e-+2H2O=Pb+40H-
C. 电解过程中左室水的电离程度减弱(忽略溶液温度变化)
D. 与传统无膜电解法相比,该电解方法可提高铅元素利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭的2 L容器中装有4 mol SO2和2 mol O2,在一定条件下开始反应。2 min末测得容器中有1.6 mol SO2,请计算:
(1)2 min末SO3的浓度;
(2)2 min内SO2的平均反应速率;
(3)2 min末SO2的转化率。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组欲设计实验验证Fe、Cu的金属活动性,他们提出了以下两种方案,请完成有关问题。
方案Ⅰ:将形状和大小均相同的铁片和铜片,分别同时放入100 mL 2.0 mol·L-1稀硫酸中,观察反应的情况,据此确定它们的金属活动性。
方案Ⅱ:利用Fe、Cu作电极设计成原电池,以确定它们的金属活动性。
(1)方案Ⅰ中发生反应的离子方程式为 。
(2)在方框内画出方案Ⅱ中的原电池装置图,注明电解质溶液名称和正、负极材料,标出电子流动方向,并写出电极反应式:
正极: ;
负极: 。
(3)结合你所学的知识,请你再设计一个与方案Ⅰ、Ⅱ不同的验证Fe、Cu活动性的简单实验方案: ,用离子方程式表示其反应原理: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2012年6月16日18时37分24秒,神舟九号成功发射。飞船的能量部分来自太阳能电池,另外内部还配有高效的MCFC型燃料电池。该燃料电池可同时供应电和水蒸气,其所用燃料为氢气,电解质为熔融的碳酸钾。已知该燃料电池的总反应为2H2+O2===2H2O,负极反应为H2+CO![]() -2e-===CO2↑+H2O,则下列推断正确的是( )
-2e-===CO2↑+H2O,则下列推断正确的是( )
A.电池工作时,CO![]() 向负极移动
向负极移动
B.电池放电时,电子经外电路由通氧气的正极流向通氢气的负极
C.正极的电极反应式为4OH--2e-===O2↑+2H2O
D.通氧气的电极为正极,发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
![]() 【题目】下列关于中和热的叙述中正确的是( )。
【题目】下列关于中和热的叙述中正确的是( )。
A.在稀溶液中,所有酸和碱反应的中和热都相等
B.在稀溶液中,强酸和强碱反应的中和热都相等
C.在稀溶液中,1 mol酸和1 mol碱反应放出的热量都相等
D.将浓硫酸滴入氢氧化钠溶液中刚好生成1 mol水时,产生的热量即为中和热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化钠样品中含有少量的杂质Na2SO4,按下列流程进行净化,流程中的( )中是合适的试剂,在[ ]中是实验操作名称。写出有关反应的化学方程式:
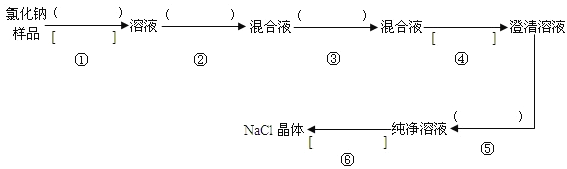
(1)操作①、②、③、⑤中所需加入试剂分别为_______、______、______、_____。
(2)操作①、④、⑥的操作名称分别为_________、_______、_______。
(3)写出有关的离子反应方程式:
第②步:_____________________________。
第⑤步:_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电化学的叙述正确的是
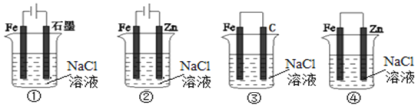
A.图①两极均有气泡产生,滴加酚酞溶液时石墨一极变红
B.图②装置可以验证牺牲阳极的阴极保护法
C.图③可以模拟钢铁的吸氧腐蚀,碳棒一极的电极反应式:O2+2H2O+4e-=4OH-
D.分别给上述4个装置的铁电极附近滴加少量K3[Fe(CN)6]溶液,②④出现蓝色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com