
把下列四种X的溶液分别加入盛有10 mL 2 mol/L盐酸的烧杯中,并均加水稀释到50 mL,此时X和盐酸进行反应,其中反应速率最大的是( )
A.20 mL 3 mol/L B.25 mL 2 mol/L
C.10 mL 4 mol/L D.10 mL 2 mol/L
科目:高中化学 来源: 题型:
下列各组中,每种电解质溶液电解时只生成氢气和氧气的是( )
A.HCl、 CuCl2、 Ba(OH)2
B.NaOH、CuSO4、 H2SO4
C.NaOH、H2SO4、 Ba(OH)2
D.NaBr、H2SO4、 Ba(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中通过如下反应制得:3SiO2+6C+2N2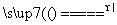 Si3N4+6CO。下列对该反应的说法正确的是( )
Si3N4+6CO。下列对该反应的说法正确的是( )
A.该反应的氧化剂是SiO2和N2
B.该反应的还原剂为CO
C.该反应的本质是有化合价变化
D.该反应中N元素被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D四种元素,已知A元素是地壳中含量最多的元素;B元素为金属元素,它的原子核外K、L层上电子数之和等于M、N层电子数之和;C元素是第3周期第一电离能最小的元素;D元素在第3周期中第一电离能最大。下列有关叙述错误的是 ( )。
A.四种元素A、B、C、D分别为O、Ca、Na、Ar
B.元素A、B、C两两组成的化合物可为CaO、CaO2、Na2O、Na2O2等
C.元素A、C简单离子的半径大小关系为A<C
D.元素B、C电负性大小关系为B<C
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室可用铁片与稀硫酸反应制取氢气,下列措施不能使氢气生成速率增大的是( )
A.加热
B.不用稀硫酸,改用质量分数为98%的浓硫酸
C.不用铁片,改用镁条
D.不用铁片,改用铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列影响化学反应速率的外界因素中,肯定能使化学反应速率加快的方法是( )
①升高温度 ②加入催化剂 ③增大反应物的物质的量
④将块状固体反应物磨成粉末 ⑤增大压强
A.①②③ B.①②④
C.①③⑤ D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.强电解质溶液一定比弱电解质溶液的导电性强
B.强电解质的稀溶液中不存在溶质分子
C.强电解质都是离子化合物,而弱电解质都是共价化合物
D.不同的弱电解质只要物质的量的浓度相同,电离程度也相同
查看答案和解析>>
科目:高中化学 来源: 题型:
现有一份NaOH固体样品,里面混有少量的Na2CO3、NaCl杂质,某同学用中和滴定的方法来测定NaOH的纯度。其操作如下:
①称取a g样品放入锥形瓶中,加水,振荡,使固体充分溶解。
②向该溶液中加入足量的BaCl2溶液,使CO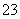 沉淀完全。
沉淀完全。
③向所得混合液中滴入2~3滴酚酞指示剂,然后用c mol·L-1的盐酸进行滴定。
④当反应达终点时,测得消耗盐酸的体积为V mL。
⑤计算样品的纯度。
试回答下面的问题
(1)滴定终点时溶液颜色如何变化:__________________________________________。
(2)第②步中生成的BaCO3沉淀未过滤出来就直接用盐酸滴定,是否会对NaoH的含量测定造成影响(填“是”或“否”)______,理由是___________________________________。
(3)第②步中生成的BaCO3沉淀未过滤出来就直接用盐酸滴定,能否改用甲基橙作指示剂(填“是”或“否”)______,理由是________________________________________。
(4)根据上述实验数据,列出计算NaOH纯度的表达式
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com