
反应:PCl5(g)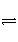
 PCl3(g)+Cl2(g)① 2HI(g)
PCl3(g)+Cl2(g)① 2HI(g)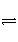
 H2(g)+I2(g)②
H2(g)+I2(g)②
2NO2(g)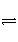
 N2O4(g)③ 在一定条件下,化学平衡时,反应物的转化率均是a%。若保持各自的温度不变、体积不变,分别再加入一定量的各自的反应物,则反应物的转化率( )
N2O4(g)③ 在一定条件下,化学平衡时,反应物的转化率均是a%。若保持各自的温度不变、体积不变,分别再加入一定量的各自的反应物,则反应物的转化率( )
A.均不变 B.均增大
C.①增大,②不变,③减小 D.①减小,②不变,③增大
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
某研究性学习小组在做制乙烯实验中,发现有“刺激性气体产物,且烧瓶中的溶液变黑色”,他们认为可能的气体产物有乙烯、二氧化碳、二氧化硫等.已知:CH3CH═CH2与酸性高锰酸钾溶液反应生成CH3COOH、CO2.

(1)实验室制乙烯实验中,下列错误操作可能引发安全事故的是 .
A.加热温度没有迅速升至170℃
B.忘记加碎瓷片
C.直接加热烧瓶
D.用医用消毒酒精
E.实验完毕,先熄灭酒精灯,后拆导管
(2)中学化学中温度计的作用有:①测定溶液温度,②测定 温度.
(3)甲同学设计如图1及图2所示装置检验该气体产物:方案Ⅰ,不能检验 二 ;方案Ⅱ,能检验 .
(4)乙同学认为制乙烯过程中,可能有CO产生,他在甲同学设计的装置后面连接如图3所示装置,探究是否有一氧化碳生成.
①乙同学应在甲同学设计的 (填“方案Ⅰ”、“方案Ⅱ”或“方案Ⅰ和方案Ⅱ”)的装置后面连接该装置;
②A瓶装的试剂是 ;
③B的硬质试管中装入 ,确认有一氧化碳生成的实验现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表示对应化学反应的离子方程式正确的是()
A. 将过量SO2气体通入氨水中:SO2+2NH3•H2O=2 NH4++SO32﹣+H2O
B. 向FeI2溶液中通入足量的氯气:2Fe2++2I﹣+2Cl2═2Fe3++I2+4Cl﹣
C. 向氢氧化钡溶液中逐滴加入少量碳酸氢钠溶液:Ba2++2OH﹣+2HCO3﹣=BaCO3↓+2H2O+CO32﹣
D. 硝酸铁溶液中滴加足量HI溶液:Fe3++3NO3﹣+12H++10I﹣=Fe2++5I2+3NO↑+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
高温下,某反应达到平衡,平衡常数K=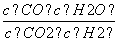 。恒容时,温度升高,H2浓度减小。下列说法正确的是( )
。恒容时,温度升高,H2浓度减小。下列说法正确的是( )
A.该反应的焓变为正值
B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小
D.该反应的化学方程式为CO+H2O
 CO2+H2
CO2+H2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对化学平衡常数K的描述中,正确的是( )
A.K越大,正反应进行的程度越大
B.温度升高,K值增大
C.反应物的转化率增大时,K值一定增大
D.平衡向逆反应方向移动时,K值减小
查看答案和解析>>
科目:高中化学 来源: 题型:
下列分离或提纯物质的方法正确的是( )
|
| A. | 用蒸馏的方法制取蒸馏水 |
|
| B. | 用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 |
|
| C. | 用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 |
|
| D. | 用加热、蒸发的方法可以除去CaCl2、MgCl2等杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列无色离子一定能大量共存的是( )
|
| A. | 0.1mol•L﹣1MgCl2溶液:K+、H+、S2﹣、Cl﹣ |
|
| B. | 0.1mol•L﹣1的Na2CO3溶液:K+、Ba2+、NO3﹣、Cl﹣ |
|
| C. | 0.1mol•L﹣1的NaOH溶液:K+、Na+、SO42﹣、CO32﹣ |
|
| D. | 1.0mol•L﹣1的KNO3溶液:H+、Fe2+、Cl﹣、SO42﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分,所列字母分别代表一种元素:

(1)m元素在周期表中的位置是
(2)下列有关说法正确的是 (填字母).
A.b、c、d元素的非金属性逐渐增强
B.f、g、h元素的原子半径逐渐减小
C.md2与bd2的化学性质类似,都具有氧化性
D.e、n的最高价含氧酸的酸性强弱:e>n
E.a、f分别与d组成的化合物中所含化学键类型完全相同
F.该表中只有4种元素组成的单质具有导电性
(3)a、c、n按原子个数比为4:1:1构成的化合物的电子式是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com