
【题目】室温下,下列事实不能说明NH3H2O为弱电解质的是( )
A.相同浓度下的NH3H2O 溶液中含有的OH﹣浓度小于 NaOH
B.相同条件下,浓度均为0.1molL﹣1NaOH溶液和氨水,氨水的导电能力弱
C.0.1molL﹣1NH3H2O能使无色酚酞试液变红色
D.OH﹣浓度相同的NH3H2O 和 NaOH 溶液分别加水稀释,c(OH﹣)随溶液体积变化的曲线如图所示,其中曲线Ⅱ是 NH3H2O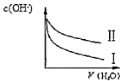
【答案】C
【解析】
抓住弱电解质的本质不完全电离及电离平衡进行突破。
A.同为一元碱且浓度相同,NaOH为强碱,完全电离,NH3H2O 溶液中含有的OH﹣浓度小于 NaOH,说明NH3H2O不完全电离,A项正确;
B.电解质溶液的导电能力与离子浓度有关,同浓度NaOH溶液和氨水,氨水的导电能力弱,反映离子浓度小,说明NH3H2O不完全电离,B项正确;
C. NH3H2O使无色酚酞试液变红色可以说明其具有碱性,无法说明是弱电解质,C项错误;
D. OH﹣浓度相同的NH3H2O 和 NaOH 溶液分别加水稀释,由于弱电解质的电离随着稀释,电离程度会变大,所以离子浓度的变化幅度会比强电解质的小,由此可知I为NH3H2O , II为NaOH,D项正确;
答案选C。


科目:高中化学 来源: 题型:
【题目】CO2是自然界碳循环中的重要物质。下列过程会引起大气中CO2含量上升的是
A. 光合作用 B. 自然降雨
C. 化石燃料的燃烧 D. 碳酸盐的沉积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:常温下,Ksp(CuS)=1.0×10-36,K sp(HgS)=1.6×10-52;pM=-lgc(M2+)。常温下,向10.0mL0.20mol·L-1Cu(NO3)2溶液中逐滴滴加0.10mo l·L-1Na2S溶液,溶液中pM与加入Na2S溶液的体积(V)的关系如图所示。下列说法错误的是

A. V0=20.0mL,m=18
B. 若c[Cu(NO3)2]=0.01mol·L-1,则反应终点可能为e点
C. a、b、d三点中,由水电离的c(H+)和c(OH-)的积最大的为b点
D. 相同条件下,若用等浓度等体积的Hg(NO3)2溶液代替上述Cu(NO3)2溶液,则反应终点b向c方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(双选)向某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应A(g) + xB(g) ![]() 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示。下列说法中正确的是( )
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示。下列说法中正确的是( )

A.30min时降低温度,40min时升高温度
B.8min前A的平均反应速率为0.08mol/(L·min)
C.反应方程式中的x=1,正反应为吸热反应
D.20min~40min间该反应的平衡常数均为4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是化学实验室中最常见的有机物,它与水互溶并有特殊香味;B的产量可衡量一个国家石油化工发展的水平。有关物质的转化关系如图所示(反应条件没有全部注明),请回答:
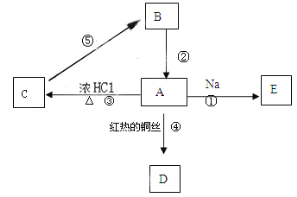
(1)有机物A的官能团名称是_______,该官能团的电子式是______。
(2)反应③的反应类型是________。
(3)反应④的化学方程式是_______。
(4)反应⑤的化学方程式是______。
(5)下列说法正确的是_______
A.反应①中Na与A的反应比Na与H2O反应更剧烈
B.反应⑤的反应类型是消去反应
C.有机物A可以使酸性高锰酸钾褪色
D.有机物B不能发生加聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式或叙述正确的是( )
A.1 mol液态肼在足量氧气中完全燃烧生成水蒸气,放出642 kJ的热量:N2H4(l)+O2(g)=N2(g)+2H2O(g) △H=+642 kJmol-1
B.C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ
C.已知:H2(g)+![]() O2(g)═H2O(l) △H=-286 kJmol-1,则:2H2O(l)═2H2(g)+O2(g)的△H=+572 kJmol-1
O2(g)═H2O(l) △H=-286 kJmol-1,则:2H2O(l)═2H2(g)+O2(g)的△H=+572 kJmol-1
D.2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1(中和热)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于 的说法正确的是( )
的说法正确的是( )
A.所有C原子有可能都在同一平面上
B.有7个碳原子可能在同一条直线上
C.该物质属于苯的同系物
D.该物质的核磁共振氢谱显示各峰面积之比为1:2:2:1:1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C12H14O2的F有机物广泛用于香精的调香剂。为了合成该物,某实验室的科技人员设计了下列合成路线:
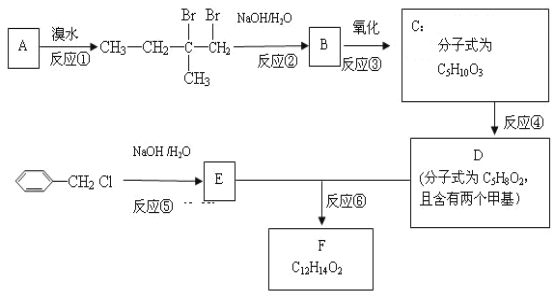
试回答下列问题:
(1)A物质在核磁共振氢谱中能呈现___种峰;
(2)C物质的官能团名称__;
(3)上述合成路线中属于取代反应的是___(填编号);
(4)写出反应①⑤的化学方程式:①___,⑤___;
由C可制备高聚物,其制备方程式为:___。
(5)已知:D分子的蒸气密度是H2密度的50倍,其红外光谱表征到碳碳双键和C=O的存在,核磁共振氢谱显示各峰面积之比为:1:1:3:3。并且该分子能与NaHCO3反应。
写出D的结构简式:___,F的结构简式:___。
(6)E属于芳香族化合物的同分异构体还有___种,其中苯环上只有3种等效氢的结构是:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是( )。
A.甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种
B.分子式符合![]() 的化合物有6种
的化合物有6种
C.已知二氯苯有3种结构,则四氯苯也有3种结构
D.菲的结构简式为 ,一定条件下,它与硝酸反应,可生成5种一硝基取代物
,一定条件下,它与硝酸反应,可生成5种一硝基取代物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com