
| A. | 0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:C(Na+)>c(CO32-)>c(HCO3- )>c(OH-) | |
| B. | 20ml 0.1mol/L CH3COONa溶液与10ml 0.1mol/L HCl溶液混合后溶液呈酸性,所得溶液中:C(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)>c(H+)>c(NH4+ )>c(OH-) | |
| D. | 0.1mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH) |
分析 A.0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合,生成碳酸钠溶液,据此分析碳酸钠溶液中离子浓度大小;
B.20ml 0.1mol/L CH3COONa溶液与10ml 0.1mol/L HCl溶液混合后反应得到等浓度的CH3COONa,CH3COOH、NaCl混合溶液,溶液呈酸性,醋酸电离大于醋酸根离子水解;
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,一水合氨存在电离平衡;
D.0.1mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积混合得到醋酸钠溶液,据溶液中质子守恒分析离子浓度.
解答 解:A.0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合,生成碳酸钠溶液,所得溶液中:C(Na+)>c(CO32-)>c(OH-)>c(HCO3- ),故A错误;
B.20ml 0.1mol/L CH3COONa溶液与10ml 0.1mol/L HCl溶液混合后反应得到等浓度的CH3COONa,CH3COOH、NaCl混合溶液,溶液呈酸性,醋酸电离大于醋酸根离子水解,C(CH3COO-)>C(Na+)>c(Cl-)>c(CH3COOH)>c(H+),故B正确;
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,一水合氨存在电离平衡,反应后一水合氨又电离出氢氧根离子和铵根离子,溶液显碱性:c(NH4+ )>c(Cl-)>c(OH-)>c(H+),故C错误;
D.0.1mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合得到醋酸钠溶液,溶液中存在质子守恒,c(OH-)=c(H+)+c(CH3COOH),故D错误;
故选B.
点评 本题考查了弱电解质电离平衡、电解质溶液中电荷守恒、物料守恒、质子守恒的分析应用,注意反应后溶液酸碱性和路致震浓度大小的比较,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 第I A族元素的化合物 | B. | 第III A族元素的化合物 | ||
| C. | 第IV A族元素的化合物 | D. | 第VII A族元素的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2+ | B. | Fe3+ | C. | Ag+ | D. | Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L水中溶解了58.5g NaCl,该溶液的物质的量浓度为1mol/L | |
| B. | V L Fe2(SO4)3溶液中含a g SO42-,取此溶液0.5VL用水稀释成2V L,则稀释后溶液的c(Fe3+)为$\frac{a}{4V}$ mol/L | |
| C. | 实验室需240mL2mol/L的CuSO4溶液,配置时应称125.0gCuSO4•5H2O | |
| D. | 10mL质量分数为98%的H2SO4,用水稀释至100mL,质量分数变为9.8% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①③⑤ | B. | ①② | C. | ②③⑤ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 酸 | 电离方程式 | 电离平衡常数K |
| CH3COOH | CH3COOH?CH3COO-+H+ | 1.76×10-5 |
| HClO | CHl0?ClO-+H+ | 3.0×10-8 |
| H2CO3 | H2CO3?H++HCO3- HCO3-?H++CO32- | K1=4.4×10-7 K2=5.61×10-11 |
| H3PO4 | H3PO4?H++H2PO4- H2PO4-?H++HPO42- HPO42-?H++HPO43- | K1=7.1×10-3 K2=6.3×10-8 K3=4.2×10-13 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 将饱和的FeCl3溶液滴入沸水中形成Fe(OH)3胶体 | |
| B. | CuSO4溶液可观察到丁达尔现象 | |
| C. | Fe(OH)3胶体可观察到丁达尔现象 | |
| D. | 胶体分散系中所有粒子的直径都不在1~100 nm之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚和甲醛在一定条件下可合成酚醛树脂 | |
| B. | 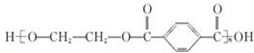 的单体是 HOCH2CH2OH 与 的单体是 HOCH2CH2OH 与  | |
| C. | 聚苯乙烯是由苯乙烯加聚生成的纯净物 | |
| D. | 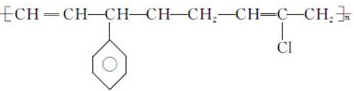 的单体有3种 的单体有3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol Na2O2和水完全反应,转移电子数为2NA | |
| B. | 0.5 L 0.2 mol•L-1 FeCl3溶液中,含Fe3+数为0.1NA | |
| C. | 在一定条件下,催化分解80 g SO3,混合气体中氧原子数为3NA | |
| D. | 常温常压下,28 g乙烯和丙烯混合气体含有的碳原子总数为2.5NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com