
| 时间/(s) | 0 | 0.01 | 0.02 | 0.03 | 0.04 |
| (CrO42-)/(mol•L-1) | 0.20 | 1.6×10-2 | 1.2×10-2 | 1.0×10-2 | |
| (Cr2O72-)/(mol•L-1) | 0 | 9.2×10-2 | 9.4×10-2 | 9.5×10-2 |
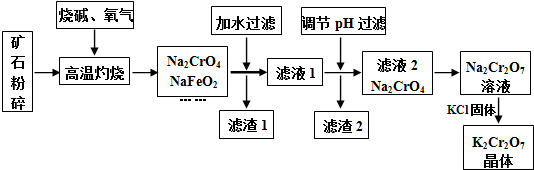
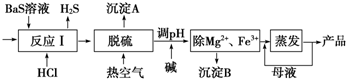
分析 铁矿中通常含有Cr2O3、FeO、Al2O3、SiO2等,将铬铁矿和烧碱、氧气混合焙烧得到Na2CrO4、NaFeO2,而SiO2与NaOH发生反应生成Na2SiO3,Al2O3与NaOH发生反应,生成NaAlO2,故还含有Na2SiO3、NaAlO2,由于NaFeO2会发生强烈水解,滤渣1中有红褐色物质,可推知NaFeO2水解生成氢氧化钠与氢氧化铁,过滤分离,滤液1中主要是NaAlO2、Na2SiO3、Na2CrO4、NaOH,滤渣1为Fe(OH)3;调节溶液pH,使NaAlO2、Na2SiO3反应转化为H2SiO3、Al(OH)3沉淀,过滤除去,滤液2主要是Na2CrO4,加入硫酸酸化,溶质变为Na2Cr2O7,然后加入KCl固体,利用溶解度不同或者受温度影响不同,结晶得到K2Cr2O7晶体,采用过滤方法得到K2Cr2O7晶体,
(1)增大反应物的表面积,加快反应速率;发生氧化还原反应,Cr2O3与O2、NaOH反应生成Na2CrO4与水;
(2)NaFeO2会发生强烈水解生成氢氧化钠与氢氧化铁;滤渣2的主要成分是氢氧化铝与硅酸;
(3)K2Cr2O7的溶解度受温度影响较大,氯化钠的溶解度受温度影响较小;
(4)①0.03s时c(Cr2O72-)=$\frac{1}{2}$×(0.2-1.0×10-2)mol/L=9.5×10-2mol/L,与0.04s时的浓度相等,故0.03s时处于平衡状态,再根据K=$\frac{c(C{r}_{2}{{O}_{7}}^{2-})}{{c}^{2}(Cr{{O}_{4}}^{2-})•{c}^{2}({H}^{+})}$计算;
②a.加少量NaHCO3固体,消耗氢离子,平衡逆向移动;
b.0.03s时处于平衡状态,不同物质表示的正逆速率之比等于其化学计量数之比;
c.平衡时各组分的浓度不一定等于化学计量数之比,与转化率等有关;
d.转化率=$\frac{浓度变化量}{起始浓度}$×100%.
解答 解:铁矿中通常含有Cr2O3、FeO、Al2O3、SiO2等,将铬铁矿和烧碱、氧气混合焙烧得到Na2CrO4、NaFeO2,而SiO2与NaOH发生反应生成Na2SiO3,Al2O3与NaOH发生反应,生成NaAlO2,故还含有Na2SiO3、NaAlO2,由于NaFeO2会发生强烈水解,滤渣1中有红褐色物质,可推知NaFeO2水解生成氢氧化钠与氢氧化铁,过滤分离,滤液1中主要是NaAlO2、Na2SiO3、Na2CrO4、NaOH,滤渣1为Fe(OH)3;调节溶液pH,使NaAlO2、Na2SiO3反应转化为H2SiO3、Al(OH)3沉淀,过滤除去,滤液2主要是Na2CrO4,加入硫酸酸化,溶质变为Na2Cr2O7,然后加入KCl固体,利用溶解度不同或者受温度影响不同,结晶得到K2Cr2O7晶体,采用过滤方法得到K2Cr2O7晶体,
(1)将矿石粉碎的目的是:增大反应物的表面积,加快反应速率;发生氧化还原反应,Cr2O3与O2、NaOH反应生成Na2CrO4与水,反应方程式为:2Cr2O3+3O2+8NaOH$\frac{\underline{\;高温\;}}{\;}$4Na2CrO4+4H2O,
故答案为:增大反应物的表面积,加快反应速率;2Cr2O3+3O2+8NaOH$\frac{\underline{\;高温\;}}{\;}$4Na2CrO4+4H2O;
(2)NaFeO2会发生强烈水解生成氢氧化钠与氢氧化铁,反应离子方程式为:FeO2-+2H2O=Fe(OH)3↓+OH-;滤渣2的主要成分是Al(OH)3和H2SiO3,
故答案为:FeO2-+2H2O=Fe(OH)3↓+OH-;H2SiO3;
(3)Na2Cr2O7溶液中加入KCl固体,降温析出K2Cr2O7的原因:K2Cr2O7的溶解度受温度影响较大,氯化钠的溶解度受温度影响较小,
故答案为:K2Cr2O7的溶解度受温度影响较大,氯化钠的溶解度受温度影响较小;
(4)①0.03s时c(Cr2O72-)=$\frac{1}{2}$×(0.2-1.0×10-2)mol/L=9.5×10-2mol/L,与0.04s时的浓度相等,故0.03s时处于平衡状态,反应达到平衡时,溶液的pH=1,该反应平衡常数K=$\frac{c(C{r}_{2}{{O}_{7}}^{2-})}{{c}^{2}(Cr{{O}_{4}}^{2-})•{c}^{2}({H}^{+})}$=$\frac{9.5×1{0}^{-2}}{(1.0×1{0}^{-2})^{2}×0.{1}^{2}}$=9.5×104,
故答案为:9.5×104;
②a.加少量NaHCO3固体,消耗氢离子,平衡逆向移动,溶液的橙色变浅,黄色加深,故a错误;
b.0.03s时处于平衡状态,v(CrO42-)(正)=2v(Cr2O72-)(逆)说明同种离子的生成熟练与消耗熟练相等,故b正确;
c.平衡时各组分的浓度不一定等于化学计量数之比,与转化率等有关,故c错误;
d.反应达到平衡时CrO42-的转化率为:$\frac{(2-1.0×1{0}^{-2})mol/L}{0.2mol/L}$×100%=95%,故d正确;
故答案为:bd.
点评 本题考查学生对工艺流程的理解、阅读题目获取信息能力、物质的分离提纯、化学平衡移动及计算等知识,题目难度中等,明确实验目的、实验原理为解答关键,试题知识点较多、综合性较强,充分考查了学生的分析、理解能力及化学实验能力.


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
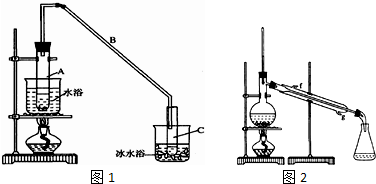
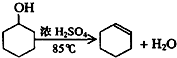
| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
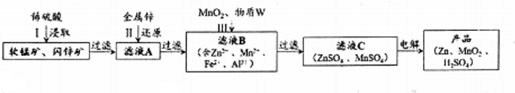
| Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
| pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
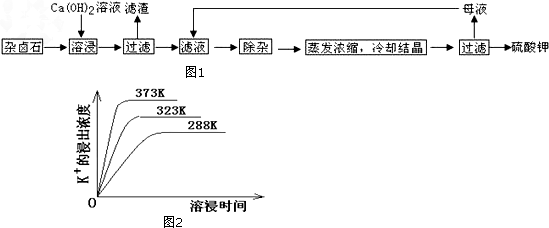
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
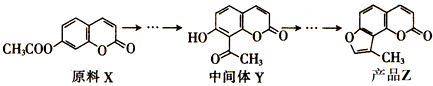
| A. | X与Y互为同分异构体 | |
| B. | X与Y均不能使酸性KMnO4溶液褪色 | |
| C. | 在光照条件下,Z中的苯环能与Cl2发生取代反应 | |
| D. | Z中所有不饱和键均能与溴发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
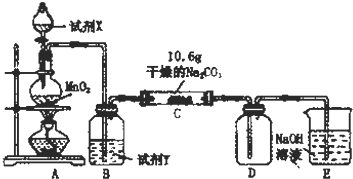
| 实验步骤 | 预期现象和结论 |
| 步骤1:取C中的少量固体样品于试管中,滴加足量蒸馏水 至固体溶解,然后将所得溶液分别置于A、B试管中. | |
| 步骤2:向A试管中滴加适量BaCl2溶液. | a.若无明显现象,证明固体中不含Na2CO3 b.若溶液变浑浊,证明固体中含Na2CO3 |
| 步骤3:向B试管中滴加过量的稀硝酸,再滴加AgNO3溶液 | 若溶液变浑浊,证明固体中含有NaCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com