
| A. | 化学键的断裂与形成一定伴随着电子的转移和能量变化 | |
| B. | 碘晶体是分子晶体,加热升华过程中只需克服分子间作用力 | |
| C. | 二氧化硅晶体属于原子晶体,每个Si通过共价键与4个O结合 | |
| D. | 氯化钠的电离是一个破坏离子键的过程 |
分析 A.成键释放能量,但不一定发生氧化还原反应;
B.I2是分子晶体,加热升华过程中,状态发生变化,分子不变;
C.SiO2晶体中每个Si原子与4个O原子以单键结合;
D.氯化钠是离子晶体.
解答 解:A.成键释放能量,但不一定发生氧化还原反应,则化学键的形成一定伴随着能量变化,不一定存在电子的转移,故A错误;
B.I2是分子晶体,加热升华过程中,状态发生变化,分子不变,只需克服分子间作用力,故B正确;
C.SiO2晶体中每个Si原子与4个O原子以共价键结合,故C正确;
D.氯化钠溶于水,只有离子键断裂,故D正确;
故选A.
点评 本题考查化学键、晶体类型,熟悉常见物质中的化学键并能举例即可解答,题目难度不大.


科目:高中化学 来源: 题型:解答题
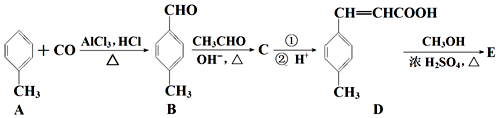
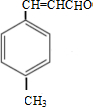 ;D→E的反应类型为酯化反应.
;D→E的反应类型为酯化反应.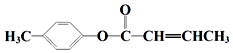 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为
是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为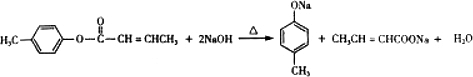 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSO3 | B. | NaOH和Na2SO3 | C. | Na2SO3 | D. | Na2SO3和NaHSO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 离子种类 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.4g乙烯和丙烯混合气体中含有C-H键的数目为0.2NA | |
| B. | 0.10molFe粉与足量水蒸气反应生成的H2分子数为0.10NA | |
| C. | 标准状况下,11.2LCO2与足量Na2O2反应,转移的电子数为NA | |
| D. | 若将1mol氧化铁完全转化为氢氧化铁胶体,则分散系中胶体粒子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S$→_{点燃}^{O_{2}}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | |
| B. | Al2O3$→_{△}^{NaOH}$NaAlO2(ap)$\stackrel{CO_{2}}{→}$Al(OH)3(s) | |
| C. | Fe$→_{高温}^{H_{2}O}$Fe2O3$\stackrel{盐酸}{→}$FeCl3(ap) | |
| D. | Cu$→_{H_{2}SO_{4},△}^{O_{2}}$CuSO4(ap)$→_{△}^{过量NaOH(ap),葡萄糖}$CuO(s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验操作 | |
| A | 制备Fe(OH)3胶体 | 将NaOH浓溶液滴加到热饱和FeCl3溶液中 |
| B | 由MgCl2溶液制备无水MgCl2 | 将MgCl2溶液加热蒸干 |
| C | “侯氏制碱法”过程中制取NaHCO3 | 将过量CO2通入到NH3和食盐的饱和溶液中 |
| D | 证明CH3COOH是弱酸 | 将CH3COOH与Na2CO3溶液反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com