
与F2>Cl2>Br2>I2 的变化规律(由强到弱)不符合的是( )
A.跟H2 或 H2O 反应的激烈程度 B.非金属活动性的强弱
C.氧化性强弱 D.沸点和熔点
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
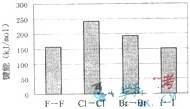 (2009?上海)海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.
(2009?上海)海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、③④ | C、①④ | D、②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深 | B、卤化氢的键长按H-F、H-C1、H-Br、H-I的顺序依次减小 | C、卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱 | D、卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易 |
查看答案和解析>>
科目:高中化学 来源: 题型:
键 | H-H | Br-Br | I-I | Cl-Cl | H-Cl | H-I | H-Br |
键能 | 436.0 | 193.7 | 152.7 | 242.7 | 431.8 | 298.7 | 366 |
(1)以上化学键中最稳定的是__________。?
(2)1 mol H2与2 mol Cl2中燃烧,放出热量__________kJ。?
(3)在一定条件下,1 mol H2与足量的Cl2、Br2、I2分别反应,放出的热量由多到少的是________。
A.Cl2>Br2>I2 B.Br2>Cl2>I2 C.Br2>I2>Cl2
(4)1 mol H2在足量的F2中燃烧比在Cl2中放热__________。
查看答案和解析>>
科目:高中化学 来源:2014届甘肃徽县一中高一下学期第一次教学质量检测化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.对于元素周期表的第一主族而言,从上到下与水反应越来越剧烈,说明从上到下金属性依次增强
B. 因为KOH的碱性强于NaOH,所以金属性Na强于K
C. 已知F2 、Cl2、Br2、I2与H2化合越来越难说明非金属性依次减弱
D. HI的还原性强于HBr,所以非金属性I强于Br
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com