
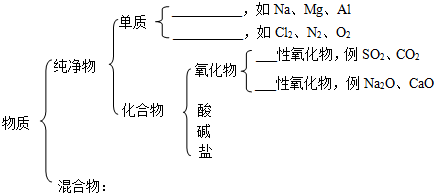


科目:高中化学 来源: 题型:

| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、31g仅含有少量白磷,无其他杂质的红磷样品中,共含有NA个磷原子 |
| B、假设1mol氯化铁完全转化为氢氧化铁胶体,则分散系中胶体微粒数小于NA |
| C、1molNa2O2与水反应转移的电子数为NA |
| D、58.5g的氯化钠固体中含有NA个氯化钠分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、澄清的石灰水与盐酸反应 Ca(OH)2+2H+═Ca2++2H2 O |
| B、钠与水的反应 Na+2H2 O═Na++2OH-+H2↑ |
| C、铜片插入硝酸银溶液 Cu+Ag+═Cu2++Ag |
| D、大理石溶于醋酸 CaCO3+2CH3COOH═Ca2++2CH3COO-+H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分散系只包括溶液和胶体 |
| B、电解质和非电解质构成所有的物质 |
| C、相同体积的两溶液,物质的量浓度大的溶液含有溶质的质量就越大 |
| D、单位物质的量的物质所具有的质量叫摩尔质量,摩尔质量与1mol物质的质量数值相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子是不断运动的 |
| B、分子能保持物质的化学性质 |
| C、分子之间有间隙 |
| D、分子是由原子构成的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、262.6 kJ?mol-1 |
| B、-131.3 kJ?mol-1 |
| C、-352.3 kJ?mol-1 |
| D、131.3 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
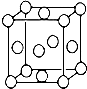 某配位化合物为深蓝色晶体,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4:4:5:1:1. 其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-1)dn+6nsl,回答下列问题.
某配位化合物为深蓝色晶体,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4:4:5:1:1. 其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-1)dn+6nsl,回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com