
对于某些离子的检验及结论一定正确的是( )
A.加入硝酸银溶液产生白色沉淀,则一定有Cl-
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO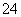
C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH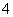
D.通入氯气,然后加入硫氰化钾溶液,溶液变为红色,一定含有Fe2+
科目:高中化学 来源: 题型:
(Ⅰ)某化学实验小组为确定过氧化氢分解的最佳催化条件,用如图装置进行实验,反应物用量和反应停止的时间数据如下表:
|
时间 H2O2 | 0.1 g | 0.3 g | 0.8 g |
| 10 mL 1.5% | 223 s | 67 s | 56 s |
| 10 mL 3.0% | 308 s | 109 s | 98 s |
| 10 mL 4.5% | 395 s | 149 s | 116 s |
请回答下列问题:
(1)盛装双氧水的化学仪器名称是 。
(2)如何检验该套装置的气密性 。
(3)相同浓度的过氧化氢,其分解速率随着二氧化锰用量的增加而________。
(4)从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入________g的二氧化锰为较佳选择。
(5)某同学分析上述数据后认为:“当用相同质量的二氧化锰时,双氧水的浓度越小,所需要的时间就越少,亦即其反应速率越快”的结论,你认为是否正确________,理由是_______________________________________。(提示:H2O2的密度可认为近似相等)。
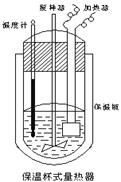 (Ⅱ)在如图所示的量热计中,将100mL 0.50mol·L-1CH3COOH溶
(Ⅱ)在如图所示的量热计中,将100mL 0.50mol·L-1CH3COOH溶
液与100mL0.55mol·L-1NaOH 溶液混合,温度从25.0℃升高到27.7℃。已知量热计的热容常数(量热计各部件每升高1℃所需的热量)是
150.5J·℃-1生成溶液的比热容为4.184J·g-1·℃-1,溶液的密度均近似
为1g·mL-1。
(1)试求CH3COOH的中和热△H= 。
(2)CH3COOH的中和热的文献值为56.1KJ· mol-1,则请你分
析在(1)中测得的实验值偏差可能的原因 。
(3)实验中NaOH过量的目的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
向NaOH和Na2CO3的混合溶液中滴加0.1mol.L-1的稀盐酸,加入盐酸的体积与生成CO2的物质的量的关系如右图所示,则原溶液中NaOH
和Na2CO3的物质的量关系为( )
A.2:1 B.1:2 C.1:1 D.3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下图转化关系。下列有关物质的推断正确的是
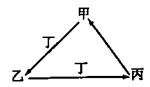
A.若甲为N2,则丁可能是O2
B.若甲为Fe,则丁可能是Cl2
C.若甲为AlCl3,则丁可能是NH3
D. 若甲为NaHCO3,则丁可能是HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
原子序数依次增大的四种元素A、B、C、D分别处于第1~4周期,其中A原子核是一个质子;B原子核外电子有6种不同的运动状态,B与C可形成正四面体形分子,D原子外围电子排布为3d104s1。请回答下列问题:
(1)这四种元素中电负性最大的是______(填元素符号,下同),第一电离能最小的是________;
 (2)C所在的主族元素气态氢化物中,沸点最低的是______(填化学式);
(2)C所在的主族元素气态氢化物中,沸点最低的是______(填化学式);
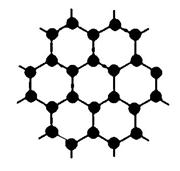
(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体结构如右图所示,其原子的杂化类型为____________;
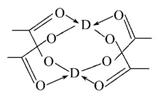 (4)D的醋酸盐晶体局部结构如右图,该晶体中含有的化学键是______(填选项序号);
(4)D的醋酸盐晶体局部结构如右图,该晶体中含有的化学键是______(填选项序号);
①极性键 ②非极性键
③配位键 ④金属键
(5)某学生所做的有关D元素的实验流程如下图:
D单质 棕色的烟
棕色的烟 绿色溶液
绿色溶液 蓝色沉淀
蓝色沉淀 蓝色溶液
蓝色溶液 黑色沉淀
黑色沉淀
请书写第⑤步反应的离子方程式:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于难溶盐MX,其饱和溶液中M+和X-的物质的量浓度之间的关系类似于[H+][OH-]=KW,存在着[M+]·[X-]=Ksp的关系。一定温度下,将足量AgCl固体分别放入下列物质中,AgCl溶解度由大到小的排列顺序为( )
①20 mL 0.01 mol·L-1 KCl溶液 ②30 mL 0.02 mol·L-1 CaCl2溶液 ③40 mL 0.03 mol·L-1 HCl溶液 ④10 mL蒸馏水 ⑤50 mL 0.05 mol·L-1 AgNO3
A.①>②>③>④>⑤ B.④>①>③>②>⑤
C.⑤>④>②>①>③ D.④>③>⑤>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,将0.01 mol CH3COONa和0.002 mol HCl溶于水,形成1 L溶液。
(1)该溶液中共含有______种不同的微粒(包括分子和离子)。
(2)在这些微粒中,________和________两种微粒的物质的量之和等于0.01 mol。
(3)________和________两种微粒的物质的量之和比H+的物质的量多0.008 mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。
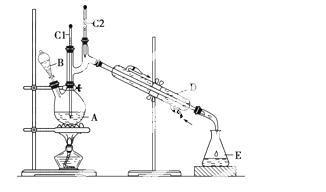
有关仪器和装置回答下列问题:
(1)上述装置图中,仪器C1和C2的名称是________,B仪器
的名称是____________,D仪器的名称是____________,E仪器的名称是______________。
(2)分液漏斗使用前必须进行的操作是________(填正确答案标号)。
a.润湿 b.干燥
c.检漏 d.标定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com